
����Ŀ��2019��6��5����������ʾ����������ȡ����ǰ�ж�����ȷ���ԿƼ�ҵ�;�������ؼ���ս���Կ��Pϡ����Ӧ���ݡ��ҹ�ϡ�������������һ���Է�̼�����Ҫ��CeFCO3����������ϡ����LnFCO3����ϡ��Ԫ��Fe��Al��Mg��SiO2�ȣ�Ϊԭ���Ʊ�CeO2��һ�ֹ���������ͼ��ʾ��

��1�����������ա�ǰ�轫��ʯ�����ϸ��������Ŀ����_________________________________�����������ա�ʱ��CeFCO3������ϡ����LnFCO3�ֱ�ת��ΪCeO2��Ln2O3����д�����ɵ�CeO2��ѧ����ʽΪ��________________________��
��2�����Ȼ������̵�Ŀ���ǽ�CeO2��Ln2O3�ֱ�ת��Ϊ�����Ե�CeCl3��LnCl3����ȥFe2O3��Al2O3��MgO��SiO2�����ʡ�����Һ��c(Ce3+)=0.01mol/L��Ϊȷ��������Ce(OH)3����������Һ��pH________����pH�ķ�Χ��������֪Ksp[Ce(OH)3=1.0��10-20]��
��3��CeO2��Ln2O3������м���ϡ���ᣬLn2O3�ܽ�����LnOCl�Ļ�ѧ����ʽΪ��___________________________________________________��
��4����������������ѡ��
�١��Ȼ���������ѡ��
���������պ��̼�����Ȼ�藺�1:3��1:4��1:5��1:6��1:7�����Ȼ�ϣ���325������ձ���60min��ϡ����������ת����ϡ���Ȼ�����Ȼ�����ͼ��ʾ��

�������պ��̼�����Ȼ�淋����������Ϊ________��
�ڡ�������������ѡ��
���������У���Ӧ�¶ȡ���Ӧʱ��Ի��ϡ���Ȼ��������ʵĹ�ϵ��ͼ��ʾ��

����¶Ⱥ�ʱ����_________��ԭ����_________________________________________��
��5��ȡ���������еõ���CeO2��Ʒ0.4500g���������ܽ����0.1000molL-1FeSO4����Һ�ζ����յ�ʱ���汻��ԭΪCe3+���������ʾ�����Ӧ��������25.00mL����Һ���ò�Ʒ��CeO2����������Ϊ___________��
���𰸡��������������ĽӴ��������Ӧ����� 4CeFCO3+2Na2CO3+O2 ����4CeO2+4NaF+6CO2 ��8 Ln2O3+2HCl=2LnOCl+H2O 1:6 550�� 1.0h �������£������ʸߣ��ӽ�100%�������ʸߣ��¶���Խϵͣ���Լ��Դ��ʱ��϶̣�����Ч��á� 95.56%
��������
��̼�����̼���ƺͿ������ȹ����У��ֽ����������̼�������ƺ�CeO2��Ln2O3�ȹ����ϣ������Ȼ�狀�ת��Ϊ�����Ե�CeCl3��LnCl3����ȥFe2O3��Al2O3��MgO��SiO2�����ʣ������������ٴλع�CeO2��Ln2O3�������ᴦ����ò�Ʒ��
��1��������������ǰ�轫��ʯ�����ϸ��������Ŀ�����������������ĽӴ��������Ӧ����֡�������������ʱ��CeFCO3������ϡ����LnFCO3�ֱ�ת��ΪCeO2��Ln2O3������������ԭ��Ӧ��֪������ʽΪ4CeFCO3+2Na2CO3+O2 ����4CeO2+4NaF+6CO2��
��2��Ksp[Ce(OH)3]=c(Ce3+)c3(OH-)=1.0��10-20������Һ��c(Ce3+)=0.01mol/L����ǡ�ò�����Ce(OH)3������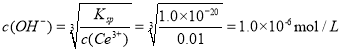 ����
����![]() ����ȷ����������������Һ��pH��8��
����ȷ����������������Һ��pH��8��
��3��CeO2��Ln2O3������м���ϡ���ᣬLn2O3�ܽ�����LnOCl������ԭ���غ�ԭ������ѧ����ʽΪ��Ln2O3+2HCl=2LnOCl+H2O��
��4����������������ѡ��
����ͼ��֪���������պ��̼�����Ȼ�淋����������Ϊ1:6��
����ͼ��֪������¶Ⱥ�ʱ����550�棬1.0h��ԭ���Ǹ������£������ʸߣ��ӽ�100%�������ʸߣ��¶���Խϵͣ���Լ��Դ��ʱ��϶̣�����Ч��á���
��5��ȡ���������еõ���CeO2��Ʒ0.4500g���������ܽ����0.1000molL-1FeSO4����Һ�ζ����յ㣬��ӦΪCeO2+Fe2++4H+= Ce3++Fe3++2H2O������25.00mL����Һ������Ӧ������CeO2�����ʵ���Ϊ0.0025mol������Ϊ0.43g���ò�Ʒ��CeO2����������Ϊ![]() ��
��


 ʱ�����������ҵԭ���ܳ�����ϵ�д�
ʱ�����������ҵԭ���ܳ�����ϵ�д� ����νӽ̲���ĩ���Ԥϰ�人������ϵ�д�
����νӽ̲���ĩ���Ԥϰ�人������ϵ�д� ������ҵ��ٳɳ����½������������ϵ�д�
������ҵ��ٳɳ����½������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ȼ���ͭ��CuCl)�㷺Ӧ���ڻ�����ӡȾ����Ƶ���ҵ��CuCl�����ڴ���ˮ��������������Ũ�Ƚϴ����ϵ���ڳ�ʪ��������ˮ���������Ժ���ͭ����Ҫ�ɷ���Cu������CuO��Ϊԭ�ϣ���������������ֽ⼼������CuCl�Ĺ��չ������£�
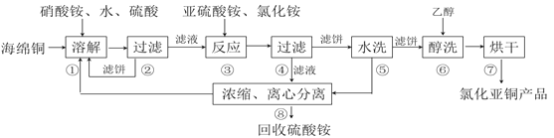
�ش��������⣺
��1���������еõ�������������_________���ܽ��¶�Ӧ������60~70�ȣ�ԭ����__________��
��2��д������������Ҫ��Ӧ�����ӷ���ʽ___________��
��3��������������pH=2����ϴ��ˮϴ������������ϴ���õ�����_________��д���ƣ���
��4�����������У�����������ʡ�ԣ�������______________________________��
��5����������������������Ҫ���й�Һ���롣��ҵ�ϳ��õĹ�Һ�����豸��__________������ĸ��
A�������� | B�����Ļ� | C����Ӧ�� | D����ʽѹ�˻� |
��6��ȷ��ȡ���Ʊ����Ȼ���ͭ��Ʒm g����������������FeCl3��Һ�У�����Ʒ��ȫ�ܽ��������ϡ���ᣬ��a mol/L��K2Cr2O7��Һ�ζ����յ㣬����K2Cr2O7��Һb mL����Ӧ��Cr2O72-����ԭΪCr3+����Ʒ��CuCl����������Ϊ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼���������������г���������Ԫ�أ�������ѧ֪ʶ�ش��������⣺
��1����ԭ�ӻ�̬ʱ��������Ų�ʽΪ__�����Ȼ������۵�306�桢�е�315�棬�ɴ��ж����Ȼ�������___���塣
��2��̼�ĵ縺�Ա���__(����������С���������")��̼��������Ԫ�ص�һ�������ɴ�С��˳��Ϊ__(��Ԫ�ط���)��
��3����Ԫ���������ڵ�8��Ԫ�صĵ����۵���ͼ��ʾ�����������8������__(��Ԫ�ط���)���γ�����������Ӧˮ����������ǿ����__(��ͼ�е����)��
��4��CS2���ӵĿռ乹��Ϊ__��Cԭ�ӵļ۲���Ӷ���Ϊ__��
��5����̬SO3�������廷״�ṹ��ͼ��ʾ���ýṹ��Sԭ�ӵ��ӻ��������Ϊ__���÷����к���___��������
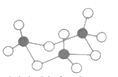
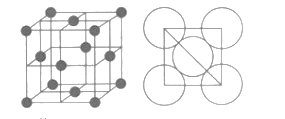
��6�������ʵľ���������ԭ��֮���λ�ù�ϵ��ͼ��ʾ������֪����ԭ�Ӱ뾶Ϊdcm��NA���������ӵ��������������ԭ������ΪM����þ�����ܶ�Ϊ__g/cm3(����ĸ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪pAg+=lgc(Ag+)��pX=lgc(X)��ij�¶��£�AgBr��AgCl��ˮ�еij����ܽ�ƽ��������ͼ��ʾ������˵���������
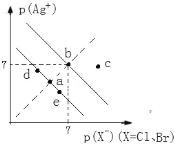
A. a��c�����Kw��ͬ
B. Ksp(AgCl)=1.0��1014 mol2��L2
C. ��AgCl��Һ�м���NaCl���壬��ʹa��䵽d��
D. AgCl(s)��Br(aq)![]() AgBr (s)��Cl(aq)ƽ�ⳣ��K=Ksp(AgCl)/Ksp(AgBr)
AgBr (s)��Cl(aq)ƽ�ⳣ��K=Ksp(AgCl)/Ksp(AgBr)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������A��B��C�������壬A���ܶ���С�����壬B��ͨ������³ʻ���ɫ��������A������B�а�����ȼ������C��������Bͨ�뵽����ʯ�����п��Եõ���ɫ������D����ݴ˻ش��������⣺
(1)д�����и���Ӧ�Ļ�ѧ����ʽ
�ٴ�����A��B�а�����ȼ������C_______________
�ڽ�����Bͨ�뵽ˮ�У�__________��
�۽�����Bͨ�뵽NaOH��Һ�У�_______________________
�ܽ�����Bͨ�뵽����ʯ�����У�_______________________
(2)����������ֱ�ͨ��������������Һ�У����ְ�ɫ������������________(����ĸ��ʾ)��
(3)����ɫ������D����ˮ�õ�������Һ���ֱ�ȡ�����ó���Һ���ݡ�
�����һ���еμ�̼������Һ�۲쵽���ֳ�����������Ӧ�Ļ�ѧ����ʽΪ______________��________��
����ڶ�����Һ�еμ������ữ����������Һ����۲쵽____________(������)��
�۰�ɫ������D�����Ư�����ֳ�Ϊ______________���������ڿ��������ױ��ʵ�ԭ��Ϊ_______________(�û�ѧ����ʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2020�꣬��ʡ����������״�����������飬����Ӱ��������Ľ����������Τ������ͷ���������Ч���������Τ�Ľṹ��ʽ��ͼ��ʾ�������й������Τ��˵����ȷ����
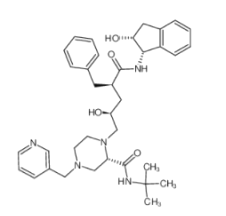
A.�����к������������ǻ����Ȼ�B.�����ϵ�һ�����ֻ������
C.���Է���ȡ����Ӧ�ͼӳɷ�ӦD.�÷������ںϳɸ߷��ӻ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2019���ǡ����ʻ�ѧԪ�����ڱ��ꡱ��W��X��Y��Z��Ϊ������Ԫ�أ�ԭ�������������ӣ�����W��X��Z��ɵĻ�����M��N��R֮�������ͼ��ʾ�ķ�Ӧ������������ȷ����
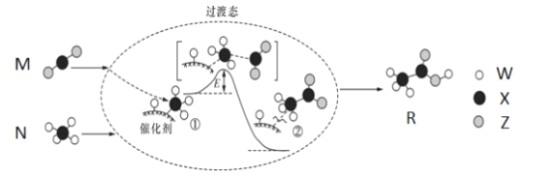
A.Ԫ�طǽ����Ե�˳��ΪX>Y>Z>W
B.M��N��R���ַ����У�����ԭ�Ӿ�����8�����ȶ��ṹ
C.M��N��R���ַ��Ӿ����м��Լ��ͷǼ��Լ�
D.W��X��Y��Z����Ԫ�ؼȿ��γ����ӻ�����ֿ��γɹ��ۻ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������Ϣ������������ȷ���ǣ� ��
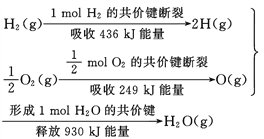
A. 2 mol H2(g)�� 1 mol O2(g)��Ӧ���� 2 mol H2O(g)��������Ϊ490 kJ
B. ��ѧ��Ӧ�������仯�Ĵ�С�뷴Ӧ�������������
C. 1 mol H2(g) ��0.5mol O2(g) ��Ӧ���� 1 mol H2O(l)�ͷ�����Ϊ245 kJ
D. 2molH2O (g)��������2 mol H2(g)��1 mol O2(g)������֮�͵�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�ȡ0.1mol/L��NaA��NaB��������Һ��1L���ֱ�ͨ��0.02molCO2���������·�Ӧ��NaA+CO2+H2O=HA+NaHCO3��2NaB+CO2+H2O=2HB+Na2CO3����1LHA��HB����Һ�ֱ��ˮϡ�������ΪVLʱ��������ͼ���ߣ�������˵����ȷ���ǣ� ��
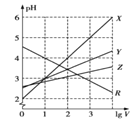
A.X��HA��Y��HB
B.������pH��NaA��Һ>NaB��Һ
C.�������£�Ũ�Ⱦ�Ϊ0.1mol/L��NaA��HA�Ļ����ҺpH>7����c(A-)>c(HA)
D.�ڵ�Ũ�ȵ�NaA��NaB�����Һ��ͨ��HCl������ʱ��c(Cl-)=c(HA)+c(HB)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com