
����Ŀ����Ԫ������A��һ�ֽ�ǿ�Ļ�ԭ���������ô���������Һ�����İ����Ƶã�64gA��ȫȼ�յõ�4.48L�ܶ�Ϊ1.25g��L��1������B(������ܶȾ��ڱ�״���²ⶨ)��
��1��A�Ļ�ѧʽ___________________��
��2��д������������Һ�����İ����Ʊ�A�����ӷ���ʽ_________________________��A���Ʊ������а�����Ҫ������������_____________________________________��
��3��A�����ɫ��CuO��Ӧ��������B��һ��ש��ɫ�����ʣ�д���û�ѧ����ʽ__________��
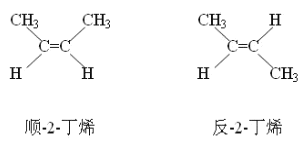
��4����֪2һ��ϩ����˳���칹(����ͼ��ʾ)������˫��ͬһ��ģ���Ϊ˳ʽ:����˫������ģ���Ϊ��ʽ�����л�����C������Ԫ����A��ͬ��Ħ������С��A��C��ͨ��A������ʵ����Ĺ�������ǡ����ȫ��Ӧ�õ���ʵ�������C���ܴ������ֽṹ����д�����ǵĽṹʽ_____________��_____________��
���𰸡�N2H4 ClO����2NH3�T N2H4��Cl��+H2O ����������ǿ�����ԣ���ֹ�������ƹ�������N2H4���� 4CuO+ N2H4�T 2Cu2O��N2��+ 2H2O ![]()
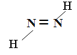
��������
��1����Ԫ������A��һ�ֽ�ǿ�Ļ�ԭ���������ô���������Һ�����İ����Ƶã�6.4gA��ȫȼ�յõ�������ܶ�Ϊ1.25g/L������B����Ħ������=1.25g/L��22.4L/mol=28g/mol��������ΪN2��A�к���NԪ�أ�Ԫ���غ��֪����Ӧ������ˮ��˵��A�л�����HԪ�أ� 4.48L���������ʵ���=![]() =0.2mol��������=0.2mol��28g/mol=5.6g����6.4gA��HԪ������=6.4g-5.6g=0.8g��Hԭ�����ʵ���=
=0.2mol��������=0.2mol��28g/mol=5.6g����6.4gA��HԪ������=6.4g-5.6g=0.8g��Hԭ�����ʵ���=![]() =0.8mol����A��N��Hԭ����Ŀ֮��=0.2mol��2:0.8mol=1:2����AΪN2H4���ʴ�Ϊ��N2H4��
=0.8mol����A��N��Hԭ����Ŀ֮��=0.2mol��2:0.8mol=1:2����AΪN2H4���ʴ�Ϊ��N2H4��
��2���������������������Ӧ����N2H4������������ԭ��Ӧ���ɿ�֪��������NaCl������Ԫ���غ��֪��ˮ���ɣ���Ӧ����ʽΪ��NaClO+2NH3�TN2H4+NaCl+H2O�����ӷ�Ӧ����ʽΪ��ClO����2NH3�T N2H4��Cl��+H2O���������ƾ���ǿ�����ԣ���������N2H4�������İ����ɷ�ֹN2H4���������ʴ�Ϊ��NaClO+2NH3�TN2H4+NaCl+H2O���������ƾ���ǿ�����ԣ���������N2H4�������İ�����ֹN2H4��������
��3��N2H4���ɫ��CuO��Ӧ����ש��ɫ������ͭ��������ˮ����Ӧ����ʽΪ��4CuO+N2H4�T2Cu2O+N2+2H2O���ʴ�Ϊ��4CuO+N2H4�T2Cu2O+N2+2H2O��
��4��������C������Ԫ����A��ͬ��Ħ������С��A��C��ͨ��A������ʵ����Ĺ�������ǡ����ȫ��Ӧ�õ������C�Ļ�ѧʽΪN2H2������2һ��ϩ����˳���칹�Ľ��ͣ����C����ԭ����˫��ͬһ��ģ���Ϊ˳ʽ����ԭ����˫������ģ���Ϊ��ʽ�����ǵĽṹʽ�ֱ�Ϊ![]() ��
�� ��
��


 �̲�ȫ���ִʾ�ƪϵ�д�
�̲�ȫ���ִʾ�ƪϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�����û������������þ���20�����ӵĸ�Ԫ�ص�ͬλ�ط��������95�����ӵ���Ԫ�أ����4�γɹ��Ƴ�4����115��Ԫ�ص�ԭ�ӡ���4��ԭ�������������˥��ɵ�113��Ԫ�ء�ǰ�ߵ�һ�ֺ���Ϊ![]() �������й�������ȷ���ǣ� ��
�������й�������ȷ���ǣ� ��
A.��Ԫ������Ԫ���Ƴɵ�115��Ԫ�����ڻ��Ϸ�Ӧ
B.113��Ԫ���������ӦΪ+3
C.����![]() ����������������֮��Ϊ174
����������������֮��Ϊ174
D.115����113��Ԫ�ص����ԭ������֮��115��113
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���뽫������������б仯��������ڶ�Ӧ�ĺ����ϣ��ٵ������������������ˮ�����Ȼ�������ˮ�����ռ��ۻ������Ȼ�������ˮ�����Ȼ�����ȷֽ⡣
��1����ѧ��û�б��ƻ�����__________�����������Ӽ��ƻ�����__________��
��2�����������Ӽ��ƻ����ַ������ۼ��ƻ�����____________________��
��3��N2�ĵ���ʽΪ__________��Na2O2�ĵ���ʽΪ___________��CO2�ĵ���ʽΪ_________��
��4���õ���ʽ��ʾMgCl2���γɹ��� _____________________��
��5����֪��1 mol H��H����1 mol N��N��1 mol N��H���ֱ���Ҫ���յ�����Ϊ436 kJ��946 k J��391 k J������N2��H2��Ӧ����1 mol NH3 ��Ҫ�ų�_____��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ������SO2��g����O2��g��ͨ�����Ϊ2L�ĺ����ܱ������У��ڲ�ͬ�¶��½��з�Ӧ���õ��±��е��������ݣ�����˵����ȷ���ǣ�������
ʵ�� ��� | �¶�/�� | ƽ�ⳣ�� /mol��1L | ��ʼ��/mol | ƽ����/mol | ||
SO2 | O2 | SO2 | O2 | |||
1 | T1 | K1 | 4 | 2 | x | 0.8 |
2 | T2 | K2 | 4 | 2 | 0.4 | y |
A. x��2.4��y��0.2 B. T1��T2�Ĵ�С��T1��T2
C. K1��K2�Ĵ�С��K1��K2 D. T1��ʱ������ʼ��������K1��K2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ���� K3[Fe(C2O4)3]��3H2O�Ǵ���ɫ���壬��421��553��ʱ���ֽ�ΪFe2O3��K2CO3��CO��CO2��H2O��ʵ�����ɲ�����������(FeC2O4��H2O)�������(K2C2O4)������(H2C2O4)��˫��ˮ(H2O2)����Ʊ�����ش���������
��1��д��H2O2�ĵ���ʽ:____________________
��2����ƽ�÷���ʽ____FeC2O4��H2O+___H2O+ __K2 C2O4+__H 2C2O4=__K3[Fe(C2O4)3]��3H2O
��3���Ʊ�������Ҫ��ֹ���ᱻH2O2��������д�����ᱻH2O2�����Ļ�ѧ��Ӧ����ʽ______��
��4���������ȶ��Կ������ȶ�����K����������Cu2++4NH3��[Cu(NH3)4]2+�����ȶ���������ʽΪ:![]() ����֪K[Fe(C2O4)3]3��=1020�� K[Fe(SCN)3]=2
����֪K[Fe(C2O4)3]3��=1020�� K[Fe(SCN)3]=2![]() 103���ܷ���KSCN��Һ����K3[Fe(C2O4)3]��3H2O�е���Ԫ��?______(����������������)��ѡ������������Ƽ�����Ԫ�صķ���_________________________________________��
103���ܷ���KSCN��Һ����K3[Fe(C2O4)3]��3H2O�е���Ԫ��?______(����������������)��ѡ������������Ƽ�����Ԫ�صķ���_________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ؽ��ij������ڹؽڻ�Һ���γ������ƾ�������NaUr����ƽ���ϵΪ��Ur��(aq)+Na+(aq) ![]() NaUr(s)������Ur����ʾ��������ӡ�ҽ���������ؽ��ײ���Ҫע�Ᵽů���ر����ֽŵ��������Զ�IJ�λ����Ϊ��һ�ιؽ��ķ���������ָ���ֺ�Ĺؽڴ�����˵��
NaUr(s)������Ur����ʾ��������ӡ�ҽ���������ؽ��ײ���Ҫע�Ᵽů���ر����ֽŵ��������Զ�IJ�λ����Ϊ��һ�ιؽ��ķ���������ָ���ֺ�Ĺؽڴ�����˵��
A. �γ������ƾ���ķ�ӦΪ���ȷ�Ӧ B. �γ������ƾ���ķ�ӦΪ���ȷ�Ӧ
C. �������ܽ�Ƚϴ� D. �����ƾ���һ��������ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ס��ҡ����������������У��ס��ҡ�����������ͬ��ij��Ԫ�أ�����֮���������ת����ϵ��![]() �������й����ʵ��ƶϲ���ȷ����
�������й����ʵ��ƶϲ���ȷ����
A. ����ΪCl2����������B. ����ΪNH3������������
C. ����ΪAlCl3��Һ�������ǰ�ˮD. ����ΪNaOH��������SO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ���ܱ�ʾ��ط�Ӧ�����������ʵ����ı仯����(�ᡢ�����굥λ��mol) ( )��
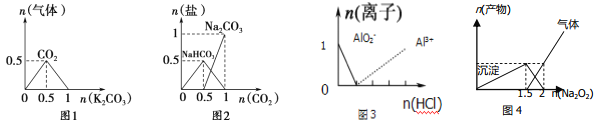
A��ͼ1��n(HCl)=l mol��K2CO3���뵽HCl��Һ�У��ڱֿ����������ɵ�����
B��ͼ2��n(NaOH)=1mol��CO2ͨ�뵽NaOH��Һ�з�Ӧ���ɵ���
C��ͼ3��n(NaAlO2)=1 mol��HCl���뵽NaAlO2��Һ�����ӵĴ������
D��ͼ4��n(AlCl3)=1 mol��Na2O2����AlCl3��Һ��Ӧ�IJ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������滷�����ͨ�����з�Ӧ���ɣ�
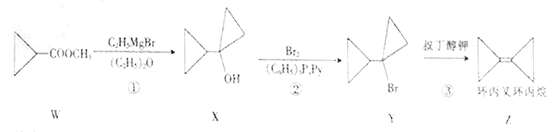
����˵������ȷ����
A. ��Ӧ������ȡ����Ӧ
B. Z�뱽��Ϊͬ���칹��
C. Z����������̼ԭ�Ӵ���ͬһƽ��
D. ��W��Ϊͬ���칹�����״�����������8��(�����������칹)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com