
����Ŀ��������ʵ��ܶȻ��������±���25�棩��
���� | Mg��OH��2 | CH3COOAg | AgCl | Ag2CrO4 |
Ksp����λ�ԣ� | 1.1��10��11 | 2.3��10��3 | 1.8��10��10 | 1.9��10��12 |
�����й�˵���в���ȷ����
A. Ũ�Ⱦ�Ϊ0.2 molL��1��AgNO3��Һ��CH3COONa��Һ��������һ������CH3COOAg����
B. ��0.001 molL��1��AgNO3��Һ����0��001 molL��1��KCl��0.001 molL��1 ��K2CrO4�����Һ�У��Ȳ���Ag2CrO4����
C. 0.11 molL��1��MgCl2��Һ�м��백ˮ����Mg��OH��2����ʱ��Һ��pHΪ9
D. ������������������������AgClˮ��Һ�м���NaCl��Һ��Ksp��AgCl������
���𰸡�B
�����������������A��Ũ�Ⱦ�Ϊ0��2 mol��L-1��AgNO3��Һ��CH3COONa��Һ�������Ϻ�Ũ�Ⱦ���Ϊ0.1mol/L����ʱc(Ag��)��c(CH3COO��)��0.01mol/L��2.3X10-3������һ������CH3COOAg������A��ȷ��B.�����Ȼ������������ܶȻ�������֪�������Ӻ��������Ũ�Ⱦ�Ϊ0.001mol/L�������¿�ʼ���ֳ���ʱ�����ӵ�Ũ�ȷֱ�Ϊ1.8X10-7mol/L��![]() mol/L�����Խ�0.001 mol��L-1��AgNO3��Һ����0��001 mol��L-1��KCl��0.001 mol��L-1��K2CrO4�����Һ���Ȳ���AgCl������B����C.����������þ���ܶȻ�������֪0.ll mol��L-1��MgCL2��Һ�м��백ˮ����Mg(OH)2����ʱ��Һ����������Ũ��Ϊ
mol/L�����Խ�0.001 mol��L-1��AgNO3��Һ����0��001 mol��L-1��KCl��0.001 mol��L-1��K2CrO4�����Һ���Ȳ���AgCl������B����C.����������þ���ܶȻ�������֪0.ll mol��L-1��MgCL2��Һ�м��백ˮ����Mg(OH)2����ʱ��Һ����������Ũ��Ϊ![]() �����������Ũ����10��9mol/L������Һ��pHΪ9��C��ȷ��D.�ܶȻ�����ֻ���¶��й�ϵ�����������������������£���AgClˮ��Һ�м���NaCl��Һ��Ksp(AgCl)���䣬D��ȷ����ѡB��
�����������Ũ����10��9mol/L������Һ��pHΪ9��C��ȷ��D.�ܶȻ�����ֻ���¶��й�ϵ�����������������������£���AgClˮ��Һ�м���NaCl��Һ��Ksp(AgCl)���䣬D��ȷ����ѡB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������(NH4)2SO4��Һ������˵����ȷ����
A. ��Һ�д��ڵ���ƽ����(NH4)2SO4![]() 2NH4++SO42-
2NH4++SO42-
B. ����Һ�еμ�����Ũ���ᣬc(NH4+)��c(SO42-)������
C. ��ˮϡ�ͣ���Һ���������ӵ�Ũ�Ⱦ���С
D. ��Һ����c(SO42-)=2c(NH4+)+2c(NH3��H2O)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������֮���ת������ͼ��ʾ��
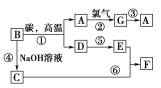
����B��������������ά�����Ӧ�ĵ��ʵĽṹ����ʯ�Ľṹ�����Ƶģ�C��F������A��������Ԫ�أ���Ӧ�����ɵ�ˮ����Ҫ���������ȥ��
(1)���Ʋ⣺A________��C________��F________��(д��ѧʽ)
(2)��д����Ӧ�����ӷ���ʽ��_________________________��
(3)�ڷ�Ӧ���У�̼��������____________________��������1 mol Aʱ��ת�Ƶ��ӵ����ʵ���Ϊ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ��̽��FeSO4��Cu(NO3)2�Ļ�����и���ֵĺ�����������������̣�
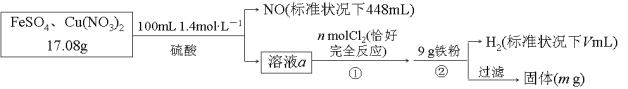
��������������ȷ���ǣ� ��
A. n=0.02 B. V=2240
C. m=3.2 D. ԭ�������FeSO4����������ԼΪ89%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���װ�(CH3NH2) �������백���ơ�25��ʱ����10mL1.0000mol��L-1�װ���Һ�е���0.5000mol��L-1��ϡ���ᣬ��Һ��pOH ������ϡ��������(V)��ϵ��ͼ��ʾ��
��֪��pOH=-lgc(OH-),Kb(CH3NH2��H2O)=4.0��10-4������˵����ȷ���ǣ� ��
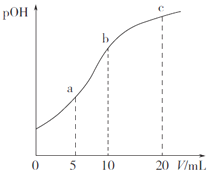
A. pOH=7 ʱ��2c(CH3NH3+)=c(SO42-)
B. ˮ�ĵ���̶ȣ�c>b>a
C. a����Һ�д��ڣ�c(CH3NH2��H2O)>c(CH3NH3+)>c(H+)>c(OH-)
D. 25��ʱ1.000 mol��L-1�װ���Һ��CH3NH2��H2O�ĵ����ԼΪ2.0%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҫ����ա�
��1������Ǧ���ص���Ȼ�����Һ�����ڳ��ʱ������ӦΪ____���ŵ����ɵĹ���ḽ���ڵ缫���棬������������������������96gʱ�������ϵ�·��ת�Ƶĵ�����Ϊ____��
��2��CO��H2һ�������·�Ӧ���ɼ״���CH3OH�����״���һ��ȼ�ϣ������ü״����һ��ȼ�ϵ�أ���ϡ�������������Һ�����ʯī���缫���õ�ظ�����ӦʽΪ_______��
��3��ijʵ��С��ͬѧ�Ե绯ѧԭ��������һϵ��̽�����
����ͼ1Ϊijʵ��С������������ԭ��Ӧ��(�����ӷ���ʽ��ʾ)_____��Ƶ�ԭ���װ��
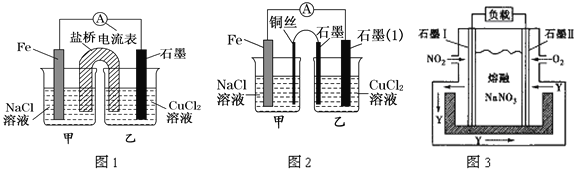
�������������䣬�������Ż�����ͭ������ʯī������n�ͣ���ͼ2��ʾ��
�ڼ�װ����ͭ�缫��ӦΪ_______________����װ����ʯī(1)Ϊ________��(��������������������������������)����װ������ͭ˿����ʯī�缫�Ϸ����ķ�ӦʽΪ_________________.
��ij����������ͼ3��ʾװ�ã�̽��NO2��O2��������N2O5�γ�ԭ��صĹ��̣��õ�ص�������ӦʽӦΪ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵ����ѡ���װ�û�����(�г�װ������ȥ)��ȷ����
ѡ�� | A | B | C | D |
ʵ�� | ��CCl4��ȡ��ˮ�е�Br2 | ��ʳ��ˮ����ȡNaCl���� | ��KI��I2�Ĺ��������л���I2 | ����100 mL 0.100 0 mol��L-1 K2Cr2O7��Һ |
װ�û����� |
|
|
|
|
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������γ�����⻯ѧ������������Ⱦ������ȼú�ͻ�����β���ǵ����������Ҫ��Դ�����ڶ����е�һЩ���������һ�����о���
��1����CH4����ԭ��������������������������Ⱦ��
��֪����CH4(g)+4NO2(g)![]() 4NO(g)+CO2(g)+2H2O(g) ��H= 574 kJ��moll
4NO(g)+CO2(g)+2H2O(g) ��H= 574 kJ��moll
��CH4(g)+4NO(g)![]() 2N2(g)+CO2(g)+2H2O(g) ��H= 1160 kJ��moll
2N2(g)+CO2(g)+2H2O(g) ��H= 1160 kJ��moll
д��CH4(g)��NO2(g)��Ӧ����N2(g)��CO2(g)��H2O(g)���Ȼ�ѧ����ʽ______________________________________________________��
��2��������β�������ܿڲ��ô�����NO��COת��������Ⱦ���塣T��ʱ���������ʵ�����NO��CO�����ݻ�Ϊ2 L���ܱ������У������¶Ⱥ�������䣬��һ�������·�����Ӧ����Ӧ������NO�����ʵ�����ʱ��仯��ͼ��ʾ��

��д���÷�Ӧ�Ļ�ѧ����ʽ______________________________________��
��10 min�ڸ÷�Ӧ������v(CO)=__________________��T��ʱ���û�ѧ��Ӧ��ƽ�ⳣ��K=_______��
�����÷�Ӧ��H��0���ں��ݵ��ܱ������У���Ӧ��ƽ��ı�ijһ����������ʾ��ͼ��ȷ����____________��������ţ�
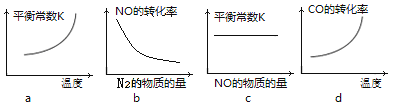
��һ���¶��£��ں����ܱ������г���һ����NO��CO���и÷�Ӧ������ѡ�����жϷ�Ӧ�Ѵﵽ��ѧƽ��״̬����____________��
a.������ѹǿ���ٱ仯 b.CO2��Ũ�Ȳ��ٱ仯
c.2v��(NO)=v��(N2) d.������ܶȲ��ٱ仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڷ�Ӧ�����г���1molA�����n molB���壬��һ�������·�����Ӧ��A������+nB������![]() mC����������ƽ��ʱ�����A��ת����Ϊ50��������ͬ�¶Ⱥ���ͬѹǿ�£�ƽ��ʱ������������Ƿ�Ӧǰ��
mC����������ƽ��ʱ�����A��ת����Ϊ50��������ͬ�¶Ⱥ���ͬѹǿ�£�ƽ��ʱ������������Ƿ�Ӧǰ�� ![]() ����n��m����ֵ�����ǣ� ��
����n��m����ֵ�����ǣ� ��
A. n=1 m=1 B. n=2 m=2
C. n=3 m=3 D. n=2 m=3
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com