
某同学弄清楚喷泉实验的原理后,有了一个创新的想法,如果改换一下烧瓶内的气体,以及胶头滴管和烧杯内的液体,也应该可以做喷泉实验。他用课本上所用的装置实际做了一下,果真得到了美丽的喷泉。下列组合中不可能是该同学设计的组合的是( )
A.氯化氢和水 B.氧气和水 C.二氧化碳和NaOH溶液 D.氯气和NaOH溶液
 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案科目:高中化学 来源: 题型:
①CaCO3(s)===CaO+CO2(g) ΔH=177.7 kJ
②C(s)+H2O(s)===CO(g)+H2(g)
ΔH=-131.3 kJ/mol
③H2SO4(l)+NaOH(l)===Na2SO4(l)+H2O(l)
ΔH=-57.3 kJ/mol
④C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ/mol
⑤CO(g)+O2(g)===CO2(g) ΔH=-283 kJ/mol
⑥HNO3(aq)+NaOH(aq)===NaNO3(aq)+H2O(l)
ΔH=-57.3 kJ/mol
⑦2H2(g)+O2(g)===2H2O(l) ΔH=-517.6 kJ/mol
(1)上述热化学方程式中,不正确的有________,不正确的理由分别是_______________________________________________________________。
(2)根据上述信息,写出C转化为CO的热化学方程式_____________。
(3)上述反应中,表示燃烧热的热化学方程式有________________;表示中和热的热化学方程式有________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
不能用于判断金属失电子能力强弱的是
A.同主族金属元素原子半径大小
B.1 mol金属单质在反应中失去电子的多少
C.水溶液中金属间发生的置换反应
D.金属元素最高价氧化物对应水化物的碱性强弱
查看答案和解析>>
科目:高中化学 来源: 题型:
柠檬酸铁可用作食品铁质强化剂、营养增补剂,用于饼干、钙质奶粉等,它可以由柠檬酸(熔点为153ºC)与氢氧化铁制得。其结构如右图。
(1)柠檬酸的晶体类型为 。
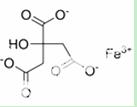 (2)柠檬酸铁中基态Fe3+的价电子排布式为 。
(2)柠檬酸铁中基态Fe3+的价电子排布式为 。
(3)柠檬酸铁所含非金属元素,电负性从小到大的顺序为
(填元素符号)。
(4)柠檬酸铁中,碳原子的杂化轨道类型为 。
(5)I2(Fe) I3(Fe)(填“>”或“<”)。
(6)柠檬酸铁溶液中不存在的微粒间作用力为 (填序号)。
A.离子键 B.极性键 C.非极性键
D.金属键 E.氢键 F.范德华力
(7)H3O+中H-O-H键角比H2O中H-O-H键角大,原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室中以下物质的贮存方法不正确的是( )
A.浓硝酸用带橡胶塞的细口、棕色试剂瓶盛放,并贮存在阴凉处
B.少量金属钠保存在煤油中
C.少量液溴可用水封存,防止溴挥发
D.保存硫酸亚铁溶液时,要向其中加入少量硫酸和铁粉
查看答案和解析>>
科目:高中化学 来源: 题型:
Na2FeO4是一种高效多功能水处理剂,应用前景广阔。一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,对此反应下列说法中正确的是( )
A.Na2O2在反应中只作氧化剂
B.O2是还原产物
C.2molFeSO4发生反应时,反应中共有8mol电子转移
D.Na2FeO4既是氧化产物又是还原产物
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质加入足量水,形成悬浊液,一段时间后,加入过量盐酸,浑浊部分消失且有无色无味气体生成的是( )
A.Ba(NO3)2和Na2SO3 B.BaCO3和Na2SO4
C.BaCl2和Na2SO4 D.Ca(HCO3)2和Ca(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
A~G是中学化学常见物质,A、D为单质,G是含A元素的酸性气体。已知:
A(s)+B(g)====C(g)+D(g) ΔH=+131.4 kJ·mol-1,
某同 学实验测知,4 g A发生上述反应吸收43.8 kJ的热量。
学实验测知,4 g A发生上述反应吸收43.8 kJ的热量。
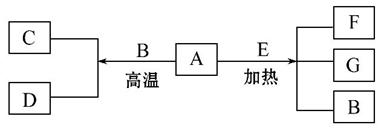
(1) 写出A元素的名称________。
写出A元素的名称________。
(2)另外知:A(s)+O2(g)====G(g) ΔH=-393.6 kJ·mol-1
C(g)+ O2(g)====G(g) ΔH=-283 kJ·mol-1
O2(g)====G(g) ΔH=-283 kJ·mol-1
D(g)+ O2(g)====B(g) ΔH=-242 kJ·mol-1
O2(g)====B(g) ΔH=-242 kJ·mol-1
由此判断“因为283 kJ·mol-1+242 kJ·mol-1>393.6 kJ·mol-1,所以A燃烧时加少量B可以放出更多的热量”这种说法是否正确?___________,理由是___[.Com ]
]
____________________________________________________。
(3)写出A+O2→C的热化学方程式:_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下表为元素周期表的一部分,参照元素①~⑦在表中的位置,请用化学用语回答下列
问题:

(1)④、⑤、⑦的原子半径由大到小的顺序为________(用元素符号表示,下同)。
(2)⑥和⑦的最高价含氧酸的酸性强弱为________>________。
(3)①、②两种元素按原子个数之比为1∶1组成的常见液态 化合物,在酸性溶液中能将Fe2+氧化,写出该反应的离子方程式__________________________________________。
化合物,在酸性溶液中能将Fe2+氧化,写出该反应的离子方程式__________________________________________。
(4)由表中元素形成的物质可发生如图中的反应,其中B、C、G是单质,B为黄绿色气体,D溶液显碱性。
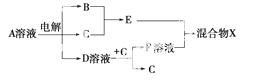
①写出D溶液与G反应的化学方程式_________________________________________
________________________________________________________________________。
②写出检验A溶液中溶质的阴离子的方法:_____________________________________
________________________________________________________________________。
③常温下,若电解1 L 0.1 mol/L的A溶液,一段时间后测得溶液pH为12(忽略溶液体积变化),则该电解过程中转移电子的物质的量为________mol。
④若上图中各步反应均为恰好完全转化,则混合物X中含有的物质有________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com