
基态铬原子的电子排布式是( )
|
| A. | 1S22S22p63S23p64S14p5 | B. | 1S22S22p63S23p63d6 |
|
| C. | 1S22S22p63S23p64S23d4 | D. | 1S22S22p63S23P63d54S1 |
考点:
原子核外电子排布.
专题:
原子组成与结构专题.
分析:
Cr的原子序数为24,核外电子数为24,根据洪特规则特例,电子排布式为1S22S22p63S23P63d54S1,以此分析.
解答:
解:A、违反了构造原理,3d能级比4p能级低,应排3d而不是4p,故A错误;
B、违反了构造原理和洪特规则特例,价电子排布部分应为d54S1,故B错误;
C、违反了洪特规则特例和核外电子式书写规范,同一能层的写在一起,应为1S22S22p63S23P63d54S1,故C错误;
D、Cr的原子序数为24,核外电子数为24,根据洪特规则特例,电子排布式为1S22S22p63S23P63d54S1,故D正确;
故选D.
点评:
本题考查原子核外电子排布,其中洪特规则及其特例是考试的热点,根据构造原理和洪特规则特例书写Cr的核外电子排布式,本题难度一般.


科目:高中化学 来源: 题型:
下列说法正确的是( )
|
| A. | 1mol任何气体所含分子数都相同,体积也都约为22.4 L |
|
| B. | 1molKClO3和1molSO2中,所含氧原子的个数比为3:2 |
|
| C. | 物质的量就是物质的摩尔质量 |
|
| D. | 在非标准状况下,1 mol任何物质的体积都不是22.4 L |
查看答案和解析>>
科目:高中化学 来源: 题型:
ClO2是一种消毒杀菌效率高、二次污染小的水处理剂.实验室可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4 2ClO2↑+K2SO4+2CO2↑+2H2O.下列说法正确的是( )
2ClO2↑+K2SO4+2CO2↑+2H2O.下列说法正确的是( )
|
| A. | KClO3在反应中得到电子 |
|
| B. | ClO2是氧化产物 |
|
| C. | H2C2O4在反应中被还原 |
|
| D. | 1mol KClO3参加反应有2 mol电子转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法错误的是( )
|
| A. | 乙醇和乙酸都是常用调味品的主要成分 |
|
| B. | 乙醇和乙酸的沸点和熔点都比C2H6、C2H4的沸点和熔点高 |
|
| C. | 乙醇和乙酸都能发生氧化反应 |
|
| D. | 乙醇和乙酸之间能发生酯化反应,酯化反应和皂化反应互为逆反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
为验证淀粉水解可生成还原性糖,进行了下列实验,该实验中操作步骤的排列顺序正确的是( )
①取少量淀粉加水制成溶液; ②加热煮沸; ③加入新制的Cu(OH)2悬浊液; ④加入几滴稀H2SO4;⑤加热; ⑥加入碱液中和并呈碱性.
|
| A. | ①④⑤⑥③② | B. | ⑤④②③①⑥ | C. | ①④②③⑤⑥ | D. | ①⑤③④⑥② |
查看答案和解析>>
科目:高中化学 来源: 题型:
在①苯 ②苯酚 ③甲苯 ④氯乙烷 ⑤乙烯 ⑥乙醇中,(填编号)
(1)一定条件下能和金属钠反应放出H2的有 ;
(2)能与NaOH溶液反应的有 ;
(3)常温下能与溴水反应的有 ;
(4)用于制取TNT的是 ;
(5)可少量掺在药皂中的是 ;
(6)能使酸性KMnO4溶液褪色的烃有 .
查看答案和解析>>
科目:高中化学 来源: 题型:
NA为阿伏伽德罗常数的值。下列叙述正确的是( )
A.常温下将28 g Fe投人到足量的浓硝酸中,可得到标准状况下33.6 L NO2
B.任何条件下,64 gSO2中含有的原子数目一定为3 NA
C.25℃时pH =13的NaOH溶液中含有OH一的数目为0. 1 NA
D.1 mo1 Na2O2反应生成O2时,必失去2 NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
FeSO4是一种精细化工产品,可用于治疗缺铁性贫血、制革、木材防腐等。制备步骤:①将3mol·L-1硫酸加入铁粉里,微热,搅拌使其充分反应;②趁热过滤;③在50℃左右蒸发、结晶,得到晶体——绿矾(FeSO4·7H2O)。回答下列问题:
(1)制备FeSO4溶液时一般不用较浓硫酸而用3mol·L-1硫酸的原因是___________
________________________________________________________________,反应时要求铁粉过量的理由是____________________________________________。
(2)检验步骤①所得溶液中金属阳离子的方法是__________________________
_________________________________________________。
(3)步骤②趁热过滤的原因是___________________________________。
(4)在空气中加热绿矾,固体质量与温度变化曲线如下图: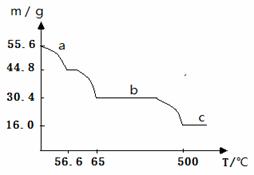
a曲线对应的反应化学方程式为___________________________________。
c曲线对应的物质化学式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
高铁酸钾( K2FeO4)是一种新型的自来水处理剂,它的性质和作用是
A.有强氧化性,可消毒杀菌,还原产物能吸附水中杂质
B.有强还原性,可消毒杀菌,氧化产物能吸附水中杂质
C.有强氧化性,能吸附水中杂质,还原产物能消毒杀菌
D.有强还原性,能吸附水中杂质,氧化产物能消毒杀菌
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com