
科目:高中化学 来源: 题型:
下列说法正确的是
A.凡是中心原子采取sp3杂化的 分子,其立体构形
分子,其立体构形 都是正四面体
都是正四面体
B.CH4分子中的sp3杂化轨道是由4个H原子的1s轨道和C原子的2p轨道混合起来而形成的
C.杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对
D.凡AB3型的共价化合物,其中心原子A均采用sp3杂化轨道成键
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A. 含有非极性键的分子不一定是共价化合物。
B. 分子间作用力比化学键弱得多,但它对物质的熔点、沸点有较大的影响,而对溶解度无影响。
C. 根据π键的成键特征判断C=C键能是C—C键能的2倍。
D. H2O中心原子采取sp杂化。
查看答案和解析>>
科目:高中化学 来源: 题型:
请完成下面两个小题:
Ⅰ.(11分)月球含有H、He、N、Na、Mg、Si等元素,是人类未来的资源宝库。
(1) 3He是高效核能原料,其原子核内中子数为___________。
(2)Na的原子结构示意图为_______,Na在氧气中完全燃烧所得产物的电子式为______。
(3)MgCl2在工业上应用广泛,可由MgO制备。
①MgO的熔点比BaO的熔点__________(填“高”或”低”)。
②月球上某矿石经处理得到的MgO中含有少量SiO2,SiO2的晶体类型为_________;所含化学键类型为 。
③MgO与碳粉和足量氯气在一定条件下反应可制备MgCl2。若尾气可用足量NaOH溶液完全吸收,则生成的盐有___________________ (写化学式)。
Ⅱ.(13分)X、Y、Z、R为前四周期元素,且原子序数依次增大。XY2是红棕色气体;X与氢元素可形成XH3;Z基态原子的M层与K层电子数相等;R2+离子的3d 轨道中有9个电子。
请回答下列问题:
(1)Y基态原子的电子排布式是________________;Z所在周期中第一电离能最大的主族元素是_________。
 (2) XY2- 离子的立体构型是_____________:R2+的水合离子中,提供孤电子对的原子是________。
(2) XY2- 离子的立体构型是_____________:R2+的水合离子中,提供孤电子对的原子是________。
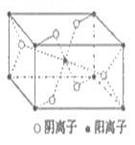
(3)Z与某元素形成的化合物的晶胞如右图所示,晶胞中阴离子与阳离子的个数比是__________。
(4)将R的硫酸盐溶液中通入足量氨气,充分反应后溶液呈
深蓝色,该反应的离子方程式是_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某烃结构简式如右图,则该有机物应命名为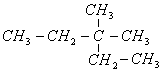
A. 2—甲基 — 2 — 乙基丁烷 B. 3 — 甲基 — 3 — 乙基己烷
C. 2,2 — 二甲基戊烷 D. 3,3 — 二甲基戊烷
查看答案和解析>>
科目:高中化学 来源: 题型:
柠檬烯是一种食用香料,其结构简式如右图。有关柠檬烯的分析正确的是
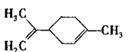
A.它的一氯代物有6种
B.它和丁基苯( 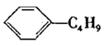 )互为同分异构体
)互为同分异构体
C.一定条件下,它分别可以发生加成、取代、氧化等反应
D.它的分子中所有的碳原子一定在同一个平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中,反应后固体物质增重的是( )
A.氢气通过灼热的CuO粉末 B.二氧化碳通过Na2O2粉末
C.将锌粒投入Cu(NO3)2溶液 D.碳酸氢钠固体加热至没有气体放出
查看答案和解析>>
科目:高中化学 来源: 题型:
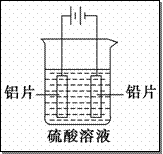 铝及铝合金经过阳极氧化,铝表面能生成几十微米厚的 氧化铝膜。某研究性学习小组模拟工业法对铝片表面进行氧化处理。分别以铅片、铝片为电极,以硫酸溶液为电解液,按照如图所示装置连接电解池装置,电解40 min后取出铝片,用水冲洗,放在水蒸气中封闭处理20~30 min,即可得到更加致密的氧化膜。下列有关说法正确的是( )。
铝及铝合金经过阳极氧化,铝表面能生成几十微米厚的 氧化铝膜。某研究性学习小组模拟工业法对铝片表面进行氧化处理。分别以铅片、铝片为电极,以硫酸溶液为电解液,按照如图所示装置连接电解池装置,电解40 min后取出铝片,用水冲洗,放在水蒸气中封闭处理20~30 min,即可得到更加致密的氧化膜。下列有关说法正确的是( )。
A.电解时电子从电源负极→导线→铝极,铅极→导线→电源正级
B.在电解过程中,H+向阳极移动,SO42-向阴极移动
C.电解过程阳极周围溶液的pH下降
D.电解的总反应为2Al+6H+===2Al3++3H2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com