
ĪļÖŹ | A | B | CO | H2 |
Č¼ÉÕČČ/kJ”¤mol-1 | 725 | 5 518 | 283 | 286 |
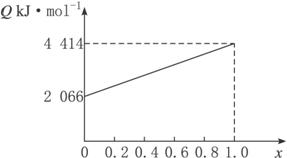
A”¢B°“²»Ķ¬±ČĄż»ģŗĻµÄČ¼ĮĻÓŠ91.2 g£¬ŌŚ×ćĮæµÄO2ÖŠČ¼ÉÕŹ±£¬·Å³öµÄČČĮæQÓėBµÄĪļÖŹµÄĮæ·ÖŹżxµÄ¹ŲĻµČēĻĀĶ¼ĖłŹ¾”£
£Ø1£©ĒóA”¢BµÄĻą¶Ō·Ö×ÓÖŹĮ攣
£Ø2£©µČĪļÖŹµÄĮæA”¢B»ģŗĻµÄČ¼ĮĻÓŠ73 g£¬ŌŚ160 L O2ÖŠĶźČ«Č¼ÉÕ£¬µĆµ½104 LĘųĢ壬Ķعż¼īŹÆ»ŅĪüŹÕŗóŹ£Óą3.2 L£ØĘųĢåĢå»ż¾łŌŚ±ź×¼×“æöĻĀ²ā¶Ø£©”£ÓÉ“ĖæÉĶʵƻģŗĻĪļÖŠŌ×ÓøöŹż±ČN£ØC£©”ĆN£ØH£©”ĆN£ØO£©ŹĒ¶ąÉŁ£æŠ“³öAŗĶBµÄ»ÆѧŹ½”£
£Ø3£©Ēó1 molÓÉA”¢BµČĪļÖŹµÄĮæ»ģŗĻ¶ų³ÉµÄČ¼ĮĻŌŚŅ»¶ØµÄŃõĘųÖŠČ¼ÉÕ£¬·Å³ö2 980 kJµÄČČĮ棬Ōņ·“Ó¦ÖŠÉś³ÉCOµÄĪļÖŹµÄĮ攣
£Ø1£©32 114 (2)9”Ć22”Ć1
A.CH4O B.C8H18 £Ø3£©0.5 mol
½āĪö£ŗ(1)øł¾ŻĶ¼Ź¾æÉÖŖ£¬µ±x=0Ź±£¬91.2 gČ«²æĪŖAĪļÖŹ£¬ĘäĶźČ«Č¼ÉշųöµÄČČĮæĪŖ2 066 kJ£¬øł¾ŻČ¼ÉÕČȵÄŗ¬ŅåÓŠ:M(A)=91.2/(2 066”Ā725)=32”£Ķ¬Ąķ£¬µ±x=1.0Ź±£¬91.2 gČ«²æĪŖBĪļÖŹ£¬¹ŹÓŠM£ØB£©=91.2/(4 414”Ā5 518)=114”£
£Ø2£©ÓÉÓŚĻą¶Ō·Ö×ÓÖŹĮæĪŖ32ĒŅÖ»ŗ¬ÓŠC”¢H”¢OČżÖÖŌŖĖŲÖŠµÄĮ½ÖÖ»ņČżÖֵĻÆŗĻĪļÖ»ÓŠCH4O·ūŗĻ£¬Ņņ“ĖAµÄ»ÆѧŹ½ĪŖCH4O”£µČĪļÖŹµÄĮæA”¢B»ģŗĻµÄČ¼ĮĻĪŖ73 gÖŠŗ¬ÓŠA£ŗ0.5 mol,B:0.5 mol,ŌŚ160 L O2ÖŠĶźČ«Č¼ÉÕŗóÉś³ÉCO2ĪŖ£Ø104 L-3.2 L£©=100 .8 L,¼“4.5 mol”£¶ųÓÉ0.5 mol CH4OČ¼ÉÕÉś³ÉCO2 0.5 mol£¬¹ŹÓÉ0.5 mol BČ¼ÉÕÉś³ÉCO2 4 mol£¬“Ó¶ųĶĘ³öŅ»øöB·Ö×ÓÖŠŗ¬ÓŠ8øöCŌ×Ó”£ŌŁøł¾ŻA”¢B¹²ĻūŗÄO2£ŗ£Ø160 L-3.2 L£©=156.8 L,¼“7 mol,“Ó¶ųĶĘ³öBµÄ·Ö×ÓŹ½ĪŖC8H18”£Č»ŗóČ·¶Ø»ģŗĻĪļÖŠŌ×ÓøöŹż±ČĪŖN£ØC£©”ĆN£ØH£©”ĆN£ØO£©=9”Ć22”Ć1”£
£Ø3£©Čē¹ū1 mol ÓÉA”¢BµČĪļÖŹµÄĮæ»ģŗĻ¶ų³ÉµÄČ¼ĮĻŌŚŃõĘųÖŠĶźČ«Č¼ÉշųöµÄČČĮæĪŖ0.5”Į725+0.5”Į5 518=3 121.5(kJ),¶ųĻÖŌŚ·Å³ö2 980 kJµÄČČĮ棬ĘäČČĮæ²īĪŖ141.5 kJ£¬ÕāÕżŹĒ0.5 mol COČ¼ÉÕĖł²śÉśµÄČČĮ棬ÓÉ“ĖæÉÖŖÉś³É0.5 mol COæɷųö141.5 kJ µÄČČĮ攣


 ŗ®¼ŁĢģµŲÖŲĒģ³ö°ęÉēĻµĮŠ“š°ø
ŗ®¼ŁĢģµŲÖŲĒģ³ö°ęÉēĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®Ķ¬ĪĀĶ¬Ń¹ĻĀ£¬H2(g)+Cl2(g)==2HCl(g)ŌŚ¹āÕÕŗĶµćČ¼Ģõ¼žĻĀµÄ”÷HĻąĶ¬
B£®Ē¦Šīµē³Ų·ÅµēŹ±µÄøŗ¼«ŗĶ³äµēŹ±µÄŅõ¼«¾ł·¢Éś»¹Ō·“Ó¦
C£®ŅŃÖŖ£ŗH2(g) + I2(g)2HI(g)£»”÷H =£9.48 kJ/mol£¬Čō½«254g I2(g)ŗĶ2gH2(g)³ä·Ö·“Ó¦æɷųö9.48 kJµÄČČĮæ
D£®ŅŃÖŖŌŚ101 kPaŹ±£¬2 gĢ¼Č¼ÉÕÉś³ÉCO·Å³öČČĮæĪŖQ kJ£¬ŌņĢ¼µÄČ¼ÉÕČČĪŖ6Q kJ”¤mol-1
”¾½āĪö”æ·“Ó¦ČČÓė·“Ó¦Ģõ¼žĪŽ¹Ų£¬AÕżČ·”£Ē¦Šīµē³Ų·ÅµēŹ±µÄÕż¼«ŗĶ³äµēŹ±µÄŅõ¼«¾ł·¢Éś»¹Ō·“Ó¦£¬B“ķĪó”£Ń”ĻīCÖŠŹĒæÉÄę·“Ó¦£¬ĖłŅŌ254g I2(g)ŗĶ2gH2(g)³ä·Ö·“Ó¦·Å³öµÄČČĮæŠ”ÓŚ9.48 kJ£¬C²»ÕżČ·”£Č¼ÉÕČČŹĒÖøŌŚŅ»¶ØĢõ¼žĻĀ£¬1molĪļÖŹĶźČ«Č¼ÉÕÉś³ÉĪČ¶ØµÄŃõ»ÆĪļŹ±Ėł·Å³öµÄÄÜĮ棬Ņņ“ĖD²»ÕżČ·”£“š°øŹĒA”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013½ģÕć½Ź”ŗ¼ÖŻµŲĒųĘߊ£ø߶žĻĀѧʌʌ֊ĮŖæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®Ķ¬ĪĀĶ¬Ń¹ĻĀ£¬H2(g)+Cl2(g)==2HCl(g)ŌŚ¹āÕÕŗĶµćČ¼Ģõ¼žĻĀµÄ”÷HĻąĶ¬
B£®Ē¦Šīµē³Ų·ÅµēŹ±µÄøŗ¼«ŗĶ³äµēŹ±µÄŅõ¼«¾ł·¢Éś»¹Ō·“Ó¦
C£®ŅŃÖŖ£ŗH2(g) + I2(g) 2HI(g)£»”÷H =£9.48 kJ/mol£¬Čō½«254g I2(g)ŗĶ2gH2(g)³ä·Ö·“Ó¦æɷųö9.48 kJµÄČČĮæ
2HI(g)£»”÷H =£9.48 kJ/mol£¬Čō½«254g I2(g)ŗĶ2gH2(g)³ä·Ö·“Ó¦æɷųö9.48 kJµÄČČĮæ
D£®ŅŃÖŖŌŚ101 kPaŹ±£¬2 gĢ¼Č¼ÉÕÉś³ÉCO·Å³öČČĮæĪŖQ kJ£¬ŌņĢ¼µÄČ¼ÉÕČČĪŖ6Q kJ”¤mol-1
”¾½āĪö”æ·“Ó¦ČČÓė·“Ó¦Ģõ¼žĪŽ¹Ų£¬AÕżČ·”£Ē¦Šīµē³Ų·ÅµēŹ±µÄÕż¼«ŗĶ³äµēŹ±µÄŅõ¼«¾ł·¢Éś»¹Ō·“Ó¦£¬B“ķĪó”£Ń”ĻīCÖŠŹĒæÉÄę·“Ó¦£¬ĖłŅŌ254g I2(g)ŗĶ2gH2(g)³ä·Ö·“Ó¦·Å³öµÄČČĮæŠ”ÓŚ9.48 kJ£¬C²»ÕżČ·”£Č¼ÉÕČČŹĒÖøŌŚŅ»¶ØĢõ¼žĻĀ£¬1molĪļÖŹĶźČ«Č¼ÉÕÉś³ÉĪČ¶ØµÄŃõ»ÆĪļŹ±Ėł·Å³öµÄÄÜĮ棬Ņņ“ĖD²»ÕżČ·”£“š°øŹĒA”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com