
【题目】(16分)止咳酮(F)具有止咳、祛痰作用。其生产合成路线如下:
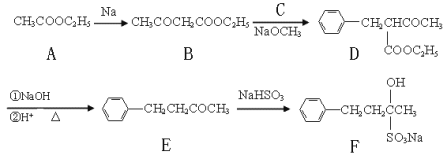
(1)写出B中含有的官能团名称: 。
(2)已知B→D反应属于取代反应,写出C(C属于氯代烃)的结构简式: 。
(3)写出E→F的反应类型: 。
(4)满足下列条件的E的同分异构体有 种。
①苯环上有两个邻位取代基; ②能与FeCl3溶液发生显色反应;
③除苯环外不含其它的环状结构。
(5)写出A→B的反应方程式: 。
(6)A→F六种物质中含有手性碳原子的是: (填物质代号)。
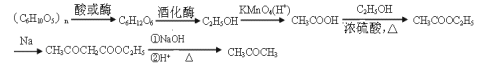
(7)目前我国用粮食发酵生产丙酮(CH3COCH3)占较大比重。利用题给相关信息,以淀粉为原料,合成丙酮。合成过程中无机试剂任选。
提示:合成路线流程图示例如下:
![]()
【答案】(1) 羰基,酯基 (2) ![]() (3) 加成 (4) 8
(3) 加成 (4) 8
(5) 2CH3COOC2H5 ![]() CH3COCH2COOC2H5+C2H5OH
CH3COCH2COOC2H5+C2H5OH
(6) D,F
(7) (4分)
【解析】(1)根据B的结构简式可知,含有的官能团是羰基,酯基。
(2)B→D反应属于取代反应,所以根据BD的结构简式可知,C是![]()
(3)E中含有羰基,但在F中变成了羟基,这说明是羰基的加成反应
(4)能与FeCl3溶液发生显色反应,说明含有酚羟基。根据分子式可知,另外一个取代基的化学式为-C4H7。即相当于是丁烯去掉1个氢原子后所得到的取代基,丁烯有3中同分异构体,总共含有8种不同的氢原子,所以-C4H7就有8种。
(5)根据AB的结构简式可知,反应应该是2分子的A通过取代反应生成1分子的B,同时还有1分子乙醇生成,方程式为2CH3COOC2H5 ![]() CH3COCH2COOC2H5+C2H5OH。
CH3COCH2COOC2H5+C2H5OH。
(6)如果和碳原子相连的4个基团各不相同,则该碳原子就是手性碳原子,所以只有饱和碳原子才可能是手性碳原子,因此根据结构简式可知DF中还有手性碳原子。
(7)考查有机物的合成,一般采用逆推法。


 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案科目:高中化学 来源: 题型:
【题目】2001年诺贝尔化学奖授予"手性碳原子的催化氢化,氧化反应"研究领域作出贡献的美,日三位科学家,手性分子具有镜像异构及光学活性,下列分子中具有光学活性的是
A.CBr2F2 B.CH3CH2OH
C.CH3CH2CH3 D.CH3CH(OH)COOH。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,等质量的 SO2 气体和 SO3 气体相比较,下列叙述中正确的是
A. 物质的量之比为 4:5 B. 密度比为 4:5
C. 体积比为 1:1 D. 原子数之比为 3:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取NaCl和KCl的混合物25g,溶于水配成溶液,加入体积为1L 0.42mol·L-1的AgNO3溶液,充分反应后过滤出沉淀,再向滤液中加入100gCu片,反应完全后,取出Cu片,洗涤干燥称其重量为101.52g,求原混合物中NaCl和KCl的物质的量各为多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸二甲酯[(CH3O)2CO]是一种具有发展前景的“绿色”化工产品,电化学合成碳酸二甲酯的工作原理如图所示(加入两极的物质均是常温常压下的物质)。下列说法正确的是
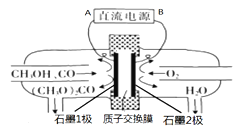
A. B为直流电源正极
B. H+由石墨2极通过质子交换膜向石墨l极移动
C. 石墨l极发生的电极反应为:2CH3OH + CO-2e= (CH3O)2CO + 2H+
D. 电解一段时间后,阴极和阳极消耗的气体的物质的量之比为l∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如右图所示。下列分析不正确的是( )

A. ①代表滴加H2SO4溶液的变化曲线
B. b点,溶液中大量存在的离子是Na+、OH–
C. c点,两溶液中含有相同量的OH–
D. a、d两点对应的溶液均显中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化物、酸、碱、盐都属于化合物。甲、乙、丙、丁、M是初中化学常见的化合物,其中甲、乙、丙、丁分属上述四种不同类别的化合物,M与甲属于同种类别的化合物。它们之间的部分转化关系如图所示(部分反应物、生成物、反应条件已略去。“—”表示物质之间能发生反应,“→”表示物质之间的转化关系)。下列推论错误的是( )
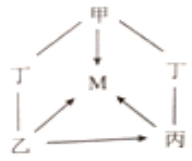
A. 若甲是碳酸钙,则可以用水鉴别乙和丙
B. 若乙可用于改良酸性土壤,则甲可以是氧化铜
C. 若丙是碳酸钠,则甲与丁溶液混合可以得到黄色溶液
D. 若丁是氢氧化钠,则甲可以通过中和反应转化为M
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳及其化合物广泛存在于自然界中,回答下列问题:
(1) 碳在形成化合物时,其键型以共价键为主,原因是___________________________。
(2) (CN)2分子中,共价键的类型有________________,C原子的杂化轨道类型是____________
(3) CO能与金属Fe形成Fe(CO)5,该化合物熔点为253K,沸点为376K,其固体属于________晶体。
(4) 与碳同族的基态Ge原子的核外电子排布式为___________,有________个未成对电子。
(5) 石墨可用作锂离子电池的负极材料,充电时发生下述反应:Li1-xC6+xLi++xe→LiC6。其结果是:Li+嵌入石墨的A、B层间。现有某石墨嵌入化合物每个六元环都对应一个Li+,写出它的化学式:_______。

(6) 碳有多种同素异形体,其中金刚石的晶体晶胞如下图所示:
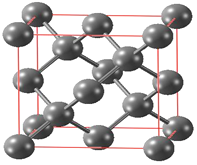
已知金刚石立方晶胞边长a pm,请计算晶体密度____________g/cm3(请用含a和NA的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关金属晶体判断正确的是
A.简单立方、配位数6、空间利用率68%
B.钾型、配位数6、空间利用率68%
C.镁型、配位数8、空间利用率74%
D.铜型、配位数12、空间利用率74%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com