
| A.与NaOH反应的氯气一定为0.3mol |
| B.n(Na+):n(Cl-)可能为7:3 |
| C.若反应中转移的电子为n mol ,则0.15<n<0.25 |
| D.n(NaCl):n(NaClO):n(NaClO3)可能为11:2:1 |


科目:高中化学 来源:不详 题型:单选题
| A.金属镁的熔点高于金属铝 |
| B.碱金属单质的熔、沸点从Li到Cs是逐渐升高的 |
| C.金属镁的硬度小于金属钙 |
| D.金属铝的硬度大于金属钠 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.反应Ⅰ原理为CO2 + NH3 + NaCl + H2O → NaHCO3↓ + NH4Cl |
| B.向饱和NaCl溶液中先通入足量的CO2,再通入足量的NH3 |
| C.反应Ⅰ生成的沉淀,经过过滤、洗涤、煅烧可得到纯碱 |
| D.往母液中通入氨气,加入细小的食盐颗粒并降温,可使氯化铵析出 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
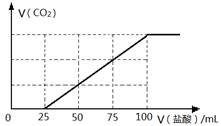
| A.原NaOH溶液的浓度为0.1 mol/L |
| B.通入CO2的体积为448 mL |
| C.所得溶液的溶质成分的物质的量之比为n(NaOH):n(Na2CO3) =" 1:" 3 |
| D.所得溶液的溶质成分的物质的量之比为n(NaHCO3):n(Na2CO3) =" 2:" 1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 是否完全沉淀的操作方法是向上层清液中继续滴加沉淀剂溶液
是否完全沉淀的操作方法是向上层清液中继续滴加沉淀剂溶液| A.①③ | B.②③ | C.②④ | D.①④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
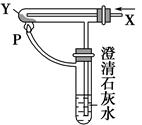
| A.H2和Fe2O3 |
| B.CO和CuO |
| C.H2和Na2CO3 |
| D.CO和Na2CO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na2O | B.Na2O2 |
| C.Na2O和Na2O2 | D.Na2O2和NaO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com