


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、W的体积分数降低 |
| B、平衡向右移动 |
| C、N的转化率提高 |
| D、反应速率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| CH3OH |
| Ⅰ |
| (1)O2 |
| (2)Zn,H2O |
| 新制Cu(OH)2 |
| H+ |
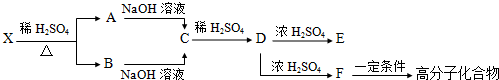
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、能发生碱性水解1mol该有机物完全反应消耗8mol氢氧化钠 |
| B、常温下,与碳酸钠溶液反应放出二氧化碳 |
| C、该有机物含有三种官能团 |
| D、与稀硫酸共热反应后混合物中有三种有机物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com