
28g KOH配成250mL溶液,溶质的物质的量 ,溶质的物质的量浓度为 。
科目:高中化学 来源:2014-2015学年福建省高一上学期第二次阶段测试化学试卷(解析版) 题型:选择题
下列溶液中氯离子的浓度与1L 1mol/L的AlCl3溶液中氯离子物质的量浓度相等的是
A、1L 1mol/L的NaCl溶液
B、1.5L 2mol/LNH4Cl溶液
C、1L 1mol/L的AlCl3溶液和1mol/L的FeCl2混合溶液
D、2L 1.5mol/L的CaCl2溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省益阳市高二上学期期中化学(文)试卷(解析版) 题型:填空题
(12分)人体内的铁不是以单质的形式存在,而是以Fe2+ 和Fe3+的形式存在。正二价铁离子易被吸收,给人补充所需铁元素时,应给予含Fe2+的亚铁盐,如硫酸亚铁。服用维生素C,可将食物中的Fe3+转变成Fe2+,有利于人体吸收。
(1)在人体中进行下列转化时  ,②中的Fe3+作 剂。
,②中的Fe3+作 剂。
(2)“服用维生素C,可将食物中的Fe3+转化成Fe2+ ”这句话指出,维生素C在这一反应中作 剂,
具有 性;某同学欲通过实验探究维生素C的这种性质,可选择的试剂是 (填字母)。
a.KI溶液 b.碘水、淀粉 c.酸性高锰酸钾溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省益阳市高二上学期期中化学(文)试卷(解析版) 题型:选择题
下列化学用语表达正确的是
A.S2-的结构示意图:
B.NaCl的电子式:
C.Cl2的结构式:Cl—Cl
D.NaHCO3的电离方程式:NaHCO3=Na+ + H+ + CO32-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省高一上学期期中化学试卷(解析版) 题型:实验题
实验室用NaOH固体配制250mL 1.25mol/L的NaOH溶液,填空并请回答下列问题:
(1)容量瓶上需标有以下五项中的 ;(3分)
①温度 ②浓度 ③容量 ④压强 ⑤刻度线
(2)配制时,其正确的操作顺序是(字母表示) ;(3分)
①用30mL水洗涤烧杯2—3次,洗涤液均注入容量瓶,振荡
②用天平准确称取所需的NaOH的质量,加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
③将已冷却的NaOH溶液沿玻璃棒注入250mL的容量瓶中
④将容量瓶盖紧,颠倒摇匀
⑤改用胶头滴管加水,使溶液凹面恰好与刻度相切
⑥继续往容量瓶内小心加水,直到液面接近刻度1—2cm处
配制时所需的主要实验仪器有 (5分)
(4)(6分)下列操作对所配溶液浓度会造成什么影响?(填“偏高”、“偏低”或“无影响”)
①用纸称量NaOH固体。 ____________;
②向容量瓶加水定容后摇匀,发现液面低于刻度线,不采取任何措施。___;
③有少量NaOH溶液残留在烧杯内。____________;
④向容量瓶加水时眼睛一直俯视液面。____________;
⑤配制前,容量瓶中有少量蒸馏水。____________;
⑥称量NaOH时,砝码错放在左盘。____________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省高一上学期期中化学试卷(解析版) 题型:选择题
实验室里需用950mL 0.1 mol/L的硫酸铜溶液时,下列操作正确的是
A.称取15.2g硫酸铜固体,加入1000 mL水
B.称取24g胆矾溶于水配成1000 mL溶液
C.称取16 g硫酸铜固体,加入1000 mL水
D.称取25 g胆矾溶于水配成1000 mL溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省高一上学期期中化学试卷(解析版) 题型:选择题
用NA表示阿伏德罗常数,下列叙述正确的是
A.标准状况下,22.4LH2O含有的分子数为 NA
B.常温常压下,1.06g Na2CO3含有的Na+的个数为0.02 NA
C.通常状况下,NA 个CO2分子占有的体积为22.4L
D.物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl- 个数为 NA
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省宁德市五校高二上学期期中化学试卷(解析版) 题型:选择题
在10 L密闭容器中,1 mol A和3 mol B在一定条件下反应:A(g)+xB(g)  2C(g),
2C(g),
2 min后达到平衡,生成0.4 mol C,测得混合气体共3.4 mol,则下列结果正确的是
A.平衡时,物质的量之比n(A)∶n(B)∶n(C)=2∶11∶4
B.x值等于3
C.A的转化率为20%
D.B的平均反应速率为0.4 mol/(L·min)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省焦作市高三上学期期中化学试卷(解析版) 题型:选择题
[化学——选修三:物质结构与性质](15分)
2011年3月11日日本发生了9.0级强地震。福岛第一核电站1号机组12日下午发生氢气爆炸。随后在爆炸核电站周围检测到的放射性物质有碘-131和铯—137,碘-131一旦被人体吸入,可能会引发甲状腺疾病。日本政府计划向核电站附近居民发放防止碘-131辐射的药物碘片。
(1)Cs(铯)的最外层电子排布式为6s1,与铯同主族的前四周期(包括第四周期)的三种元素A、B、C的电离能如下表:

那么三种元素C的元素符号为____________,形成其单质晶体的化学键类型__________。
(2)F、Cl、Br与I同主族,BeF2与H2O都是由三个原子构成的共价化合物分子,二者分子中的中心原子Be和O的杂化方式分别是________、________。与碘同主族的氯具有较高的活泼性,能够形成大量的含氯化合物,如金属氯化物,非金属氯化物等。BCl3是一种非金属氯化物,该物质分子中B—Cl键的键角为________。基态溴原子的简化电子排布式为 _____ 。
(3)卤素互化物如IBr、ICl等与卤素单质结构相似、性质相近。Cl2、IBr、ICl沸点由高到低的顺序为_______ __。
(4)测定气态氟化氢分子量总大于20,你认为可能的原因为 。
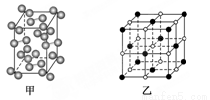
(5)碘—131是碘单质,其晶胞结构如下图甲所示,该晶胞中含有________个I2分子;KI的晶胞结构如下图乙所示,每个K+紧邻________个I-。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com