
| A、可用淀粉-KI试纸和食醋检验真假碘盐 |
| B、用饱和氯化铵溶液可以清洗金属表面的锈迹 |
| C、次氯酸钠溶液是生活中常用的消毒剂 |
| D、经常食用含明矾的食品能中和过多的胃酸 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
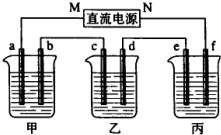 如图所示装置中,甲,乙、丙三个烧杯依次分别盛放100g5.00%nNaOH溶液、足量的CuSO4溶液和100g9.55%的K2SO4溶液,电极均为石墨电极.接通电源,经过一段时间后,测得丙中K2SO4浓度为10.00%,乙中c电极质量增加,据此回答问题:
如图所示装置中,甲,乙、丙三个烧杯依次分别盛放100g5.00%nNaOH溶液、足量的CuSO4溶液和100g9.55%的K2SO4溶液,电极均为石墨电极.接通电源,经过一段时间后,测得丙中K2SO4浓度为10.00%,乙中c电极质量增加,据此回答问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH相等的①NH4Cl ②(NH4)2SO4 ③NH4HSO4溶液中,c(NH4+)大小顺序:①=②>③ |
| B、相同条件下pH=5的①NH4Cl溶液 ②CH3COOH溶液 ③稀盐酸溶液中由水电离的c(H+):①>②>③ |
| C、常温下0.4mol/L HB溶液和0.2mol/L NaOH溶液等体积混合后溶液的pH=3,则溶液中微粒浓度大小顺序为:c(HB)>c(Na+)>c(B-)>c(H+)>c(OH-) |
| D、常温下,将醋酸钠、盐酸两溶液混合后,溶液呈中性,则混合溶液中:c(Na+)>c(Cl-)>c(CH3COOH) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、少量氯气和溴化亚铁溶液反应:C12+2Br-=2Cl-+Br2 |
| B、氢氧化钡溶液中加入少量的硫酸氢钠溶液:Ba2++H++OH-+SO42-=BaSO4↓+H2O |
| C、蛋壳溶于食醋中:CaCO3+2H+=Ca2++CO2↑+H2O |
| D、金属钠投入硫酸铜溶液中:2Na+Cu2+=Cu+2Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、由水电离出来的c(H+)=1.0×10-13mo1/L |
| B、c(CH3COOH)>c(H+)>c(CH3COO-)>c(OH-) |
| C、与同浓度的盐酸分别加水稀释10倍:pH(醋酸)>pH(盐酸) |
| D、与等浓度等体积NaOH溶液反应后的溶液中:c(CH3COOH)+c(CH3COO-)=0.1mo1/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | |
| 环境 |  |
 |
 |
 |
| 行为 | 切勿随意进入 | 严禁烟火 | 尽量远离 | 顺风向低处跑 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、溶质物质的量相等的Ba(OH)2与KAl(SO4)2?12H2O溶液混合:Ba2++6OH-+2Al3++SO
| ||||
| B、Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+═Fe3++3H2O | ||||
C、向NaAlO2溶液中通入过量CO2制Al(OH)3:AlO
| ||||
D、将适量CO2通入Ca(ClO)2溶液中:2ClO-+CO2+H2O═CO
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| 180℃ |
| 催化剂 |
| CO2 |
| 反应Ⅰ |
| Na2SO3水溶液 |
| 反应Ⅱ |
| 浓度/mol?L-1/ 时间/min |
NO | N2 | CO2 |
| 0 | 0.100 | 0 | 0 |
| 10 | 0.058 | 0.021 | 0.021 |
| 20 | 0.040 | 0.030 | 0.030 |
| 30 | 0.040 | 0.030 | 0.030 |
| 40 | 0.032 | 0.034 | 0.017 |
| 50 | 0.032 | 0.034 | 0.017 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com