
 .
.分析 B形成的化合物种类繁多,确定B为C元素;根据C、D为空气中含量最多的两种元素,且A、B、C、D、E、F的原子序数依次增大,所以C为N元素,D为O元素;D、E形成两种不同的离子化合物,则E为Na;F为同周期半径最小的元素,E、F同周期,所以F为Cl元素;它们的原子核外电子层数之和为13,则A为H元素,然后结合元素及其单质、化合物的性质来解答.
解答 解:B形成的化合物种类繁多,确定B为C元素;根据C、D为空气中含量最多的两种元素,且A、B、C、D、E、F的原子序数依次增大,所以C为N元素,D为O元素;D、E形成两种不同的离子化合物,则E为Na;则A为原子序数小于C的元素,结合题目知为H,
(1)Na元素与O按原子个数为1:1形成的化合物为Na2O2,其电子式为 ,故答案为:
,故答案为: ;
;
(2)B、D形成的化合物CO2中存在的化学键为共价键;H、C、N、O四种元素形成的化合物CA5BD3为NH5CO3,化学式为:NH4HCO3,即碳酸氢铵,碳酸氢铵含有离子键属于离子化合物,故答案为:共价;离子;
(3)A、C、D、E分别为H、N、O、Na,H是周期表中半径最小的,同周期原子序数越大半径越小,所以N>O,不同周期电子层越多半径越大,所以原子半径Na>N,则由大到小的顺序为:Na>N>O>H;故答案为:Na>N>O>H;
(4)元素B和F的分别为C、Cl,非金属性C比Cl弱,高氯酸能制备碳酸,则高氯酸的酸性大于碳酸,即非金属性,Cl大于C,故答案为:弱;
(5)元素的非金属性越强,其最高价氧化物的水化物的酸性越强,非金属性N>C,故硝酸的酸性强于碳酸,故答案为:弱.
点评 本题考查原子结构与元素周期律,元素的推断是解答本题的关键,熟悉化学用语的使用即可解答,题目难度中等.


科目:高中化学 来源: 题型:填空题
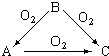 常温下某淡黄色固体单质A,与它的气态氢化物B和氧化物C之间,有如图的转变关系,请回答:(1)A是S、B是H2S、C是SO2.
常温下某淡黄色固体单质A,与它的气态氢化物B和氧化物C之间,有如图的转变关系,请回答:(1)A是S、B是H2S、C是SO2.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
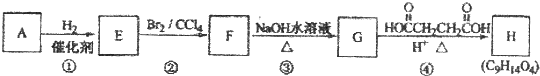
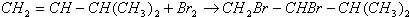 ;
;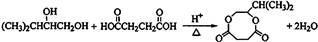 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在粗盐提纯中,当加热到蒸发皿中有较多固体析出,残留少量液体时,停止加热,用余热将液体蒸干 | |
| B. | 当振荡分液漏斗中的混合溶液时,须用一只手压住分液漏斗的玻璃塞,另一只手握住旋塞,将分液漏斗倒转过来,用力振荡 | |
| C. | 从加碘盐中获取碘单质的操作步骤为:溶解-萃取-分液-蒸馏 | |
| D. | 实验过程中若皮肤不慎沾上少量碱液,应先用大量水冲洗,再用2%醋酸溶液或饱和硼酸溶液洗,最后用水冲洗 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (对苯醌)═N2H4+
(对苯醌)═N2H4+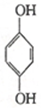 (对苯酚),N2H4的结构式为
(对苯酚),N2H4的结构式为 ,该电池正极的电极反应式为
,该电池正极的电极反应式为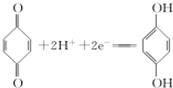 .
.| 温度/℃ | 200 | 300 | 400 |
| K | 1.0 | 0.86 | 0.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 图I表示盐酸滴加到0.1mol/L某碱溶液中得到的滴定曲线,由图I可知二者恰好中和时,所得溶液的pH=7 | |
| B. | 图II表示一定条件下进行的反应2SO2+O2?2SO3△H<0各成分的物质的量变化,t2时刻改变的条件可能是加压或降低温度 | |
| C. | 图III表示某明矾溶液中加入Ba(OH)2溶液,沉淀的质量与加入Ba(OH)2溶液体积的关系,在加入20ml Ba(OH)2溶液时,沉淀是Al(OH)3与BaSO4的混合物 | |
| D. | 图IV表示向一定体积含等浓度NH4Cl、AlCl3、MgCl2混合溶液中逐渐加入NaOH溶液至过量的过程中,生成沉淀的质量与加入NaOH溶液的体积之间的关系 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com