
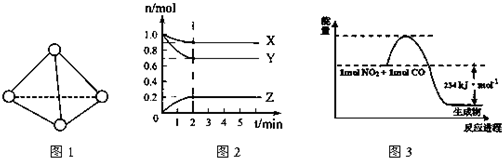
���� ��1��A���ṹ���Ƶķ��Ӿ��壬�۵�����Է������������ȣ�
B�������ʴ��ڷ��ӣ����ڷ��Ӿ��壻
C��ͬ��Ԫ�صIJ�ͬ���ʻ�Ϊͬ�������壻
D���ӽṹͼ�пɿ�����һ��N4�����к���6��N-N�������ݷ�Ӧ�ȵ��ڷ�Ӧ����ܼ��ܼ���������ܼ��ܼ��㣻
E��ͬ��Ԫ�صIJ�ͬ���ʻ�Ϊͬ�������壻
F����ͬ������N4��N2����ԭ�Ӹ�����ͬ��
��2�����ݵ����������ķ�Ӧ֮�ȣ���֪YΪ���������ݻ�ѧ��Ӧ���ʼ��㹫ʽ������
��3����Ӧ����������������������������������˷�Ӧ���ʱ䣬�����Ȼ�ѧ����ʽ����д������д���Ȼ�ѧ����ʽ��
��4����NO2��g��+CO��g��=CO2��g��+NO��g����H=-234kJ•mol-1��
��N2��g��+2NO2��g���T4NO��g������H=+292kl•mol-1��
���ݸ�˹���ɼ��㷴Ӧ�ȣ�
��� �⣺��1��A��N4����ף�P4���ṹ���ƣ���Ϊ���Ӿ��壬����N4��Է�������С��P4��������Ӽ�����������P4�����۵����P4����A����
B�������ʴ��ڷ��ӣ����ڷ��Ӿ��壬������ԭ�Ӿ��壬��B����
C��ͬ��Ԫ�صIJ�ͬ���ʻ�Ϊͬ�������壬��N4��N2��ͬ�������壬��C����
D���ӽṹͼ�пɿ�����һ��N4�����к���6��N-N��������N4��g��=2N2��g����H���С�H=6��193 kJ•mol-1-2��941 kJ•mol-1=-724 kJ•mol-1����1 mol N4����ת��ΪN2ʱҪ�ų�724 kJ��������D��ȷ��
E��ͬ��Ԫ�صIJ�ͬ���ʻ�Ϊͬ�������壬ͬλ����ԭ�ӣ���E����
F����ͬ������N4��N2����ԭ�Ӹ�����ͬ����ԭ�Ӹ�����Ϊ1��1����F��ȷ��
�ʴ�Ϊ��DF��
��2�����ݵ����������ķ�Ӧ֮�ȣ���֪YΪ������2min��N2�ķ�Ӧ���ʦԣ�N2��=$\frac{��c}{��t}$=$\frac{0.1mol}{0.5L��2min}$=0.1mol•L-1•min-1��
�ʴ�Ϊ��H2��0.1mol•L-1•min-1��
��3����ͼ���֪��Ӧ�������������������������������ڷ��ȷ�Ӧ���÷�Ӧ���ʱ��H=E1-E2=134KJ/mol-368KJ/mol=-234KJ/mol�����Ȼ�ѧ����ʽΪ��NO2��g��+CO��g��=CO2��g��+NO��g����H=-234kJ•mol-1��
�ʴ�Ϊ�����ȣ�NO2��g��+CO��g��=CO2��g��+NO��g����H=-234kJ•mol-1��
��4����NO2��g��+CO��g��=CO2��g��+NO��g����H=-234kJ•mol-1��
��N2��g��+2NO2��g���T4NO��g������H=+292kl•mol-1��
���ݸ�˹���ɣ�2����-�ڵ�2NO��g��+2CO��g���T2CO2��g��+N2��g����H=-760kJ/mol��
�ʴ�Ϊ��-760kJ/mol��
���� ���⿼���˷�Ӧ�ȵļ��㡢�Ȼ�ѧ����ʽ����д����Ӧ���ʵļ���ȣ���Ŀ�漰��֪ʶ��϶࣬�Ѷ��еȣ������ڿ���ѧ���Ի���֪ʶ���ۺ�Ӧ��������


 ABC����ȫ�ž�ϵ�д�
ABC����ȫ�ž�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Һϡ�͵�ԭ�����10�� | B�� | ���������Ĵ����ƹ��� | ||
| C�� | ��������0.2mol/L���� | D�� | �����Һ���¶� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��FeCl3��Һֱ��������ȡ��ˮFeCl3���� | |
| B�� | ����CuSO4��Һʱ�������������ϡ����������Cu2+ˮ�� | |
| C�� | ����к͵ζ�ʵ���У��ô�����Һ��ϴ��ƿ�Լ�Сʵ����� | |
| D�� | �ù㷺pH��ֽ�ⶨ��ҺpHʱ����ֽ��Ԥ��������ˮʪ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
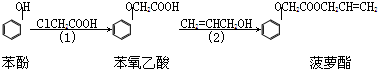
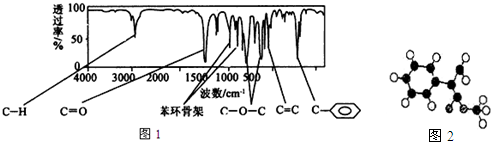
 ��ע����Ӧ��������
��ע����Ӧ���������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
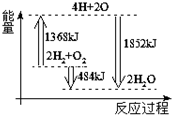
| A�� | ��H��Oԭ���γ�2 mol H2O��g����������1852 kJ���� | |
| B�� | ��2mol H2��g����1 mol O2��g���еĻ�ѧ����ΪH��Oԭ�ӣ����ų�1368 kJ���� | |
| C�� | 2mol H2��g����1 mol O2��g����Ӧ����2 mol H2O��g�������ų�484 kJ���� | |
| D�� | 2mol H2��g����1 mol O2��g����Ӧ����2 mol H2O��l����������484 kJ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʵ����� | H2O2��ҺŨ�� | H2O2��Һ�¶� | ���� | ����ʱ�� |
| �� | 5% | 20�� | 2��1mol/LFeCl3 | t |
| �� | 5% | 40�� | 2��1mol/LLFeCl3 | t |
| �� | 10% | 20�� | 2��1mol/LLFeCl3 | t |
| �� | 5% | 20�� | ��ʹ�� | t |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ȼ������� | B�� | ��ˮ�ƾ� | C�� | ���ڵ��Ȼ��� | D�� | ����ͭ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��λʱ��������n mol O2��ͬʱ����n mol NO2 | |
| B�� | ��λʱ��������n mol O2��ͬʱ����2n mol NO | |
| C�� | ���������ܶȲ��ٸı��״̬ | |
| D�� | ����������ɫ���ٸı��״̬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
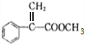 ��
��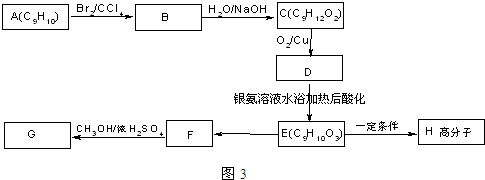
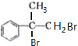 +2NaOH$��_{ˮ}^{��}$
+2NaOH$��_{ˮ}^{��}$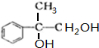 +2NaBr C��D
+2NaBr C��D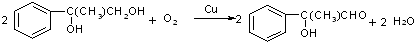 E��Hn
E��Hn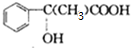 $\stackrel{һ������}{��}$
$\stackrel{һ������}{��}$ +��n-1��H2O
+��n-1��H2O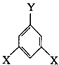 ��ʾ������X��Y����ΪH������д����������ͨʽ���ܷ���������Ӧ���������ʵĽṹ��ʽ��
��ʾ������X��Y����ΪH������д����������ͨʽ���ܷ���������Ӧ���������ʵĽṹ��ʽ��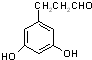 ��
��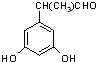 ��
��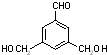 ��
��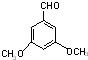 ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com