
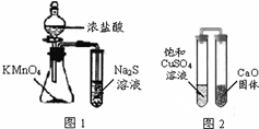
| A. | 下列有关实验原理、操作或现象不正确的是图1锥形瓶中滴入浓盐酸后充满黄绿色气体,试管中出现浅黄色浑浊 | |
| B. | 图2放置一段时间后,饱和CuSO4溶液中出现白色晶体 | |
| C. | 用玻璃棒蘸取某溶液做焰色反应实验,火焰呈黄色说明该溶液中不含钾元素 | |
| D. | 蒸馏时,将温度计水银球靠近蒸馏烧瓶支管口处 |
分析 A.高锰酸钾氧化HCl,氯气氧化硫化钠;
B.CaO具有吸水性,饱和硫酸铜溶液中有晶体析出;
C.检验钾元素应用透过蓝色钴玻璃观察;
D.蒸馏时,温度计测定馏分的温度.
解答 解:A.高锰酸钾氧化HCl生成氯气,则图1锥形瓶中滴入浓盐酸后充满黄绿色气体,氯气与硫化钠反应生成S,则试管中出现浅黄色浑浊,故A正确;
B.CaO具有吸水性,饱和硫酸铜溶液中有晶体析出,观察到蓝色晶体出现,故B错误;
C.检验钾元素应用透过蓝色钴玻璃观察,否则被黄色光遮住,故C错误;
D.蒸馏时,温度计测定馏分的温度,则将温度计水银球靠近蒸馏烧瓶支管口处,故D正确;
故选BC.
点评 本题考查化学实验方案的评价,涉及氧化还原反应、物质的性质、焰色反应、蒸馏实验等,注重基础知识的考查,注意思维严密性的训练,题目难度不大.


科目:高中化学 来源: 题型:填空题
 已知:CH3CH2OH+NaBr+H2SO4(浓) $\stackrel{△}{→}$ CH3CH2Br+NaHSO4+H2O.
已知:CH3CH2OH+NaBr+H2SO4(浓) $\stackrel{△}{→}$ CH3CH2Br+NaHSO4+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA | |
| B. | 标准状况下,14 g氮气含有的核外电子数为5NA | |
| C. | 标准状况下,5.6 L四氯化碳(CCl4)含有的分子数为0.25NA | |
| D. | NA个一氧化碳分子和0.5 mol 甲烷的质量比为7:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 学会配制一定物质的量浓度的溶液具有重要意义.某同学欲用下图试剂瓶标签上某浓度的盐酸配制450mL 0.4mol/L的稀盐酸.
学会配制一定物质的量浓度的溶液具有重要意义.某同学欲用下图试剂瓶标签上某浓度的盐酸配制450mL 0.4mol/L的稀盐酸.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol/L | B. | 0.1mol/L | C. | 0.001mol/L | D. | 10mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4Cl的电子式: | |
| B. | Cl-的结构示意图: | |
| C. | 二氧化碳的电子式:${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$C${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$ | |
| D. | 中子数为16的硫离子:${\;}_{16}^{32}$S2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①⑥⑦ | B. | ③⑧ | C. | ③⑦⑧ | D. | ⑦⑧ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com