
 室温下,将1.000mol•L-1盐酸滴入20.00mL 1.000mol•L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示.下列有关说法不正确的是( )
室温下,将1.000mol•L-1盐酸滴入20.00mL 1.000mol•L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示.下列有关说法不正确的是( )| A. | a点水的离子积Kw=1.0×10-14 | |
| B. | b点:c(NH4+)+c(H+)=c(Cl-)+c(OH-) | |
| C. | c点:c(Cl-)=c(NH4+) | |
| D. | d点后,溶液温度略下降的主要原因是NH3•H2O电离吸热 |
分析 A.a点为氨水,常温下氨水中水的离子积为1.0×10-14;
B.溶液中一定满足电荷守恒,根据电荷守恒判断;
C.c点pH=7,则c(H+)=c(OH-),溶液中电荷守恒为c(NH4+)+c(H+)=c(Cl-)+c(OH-);
D.根据d点盐酸和氨水恰好完全反应,放热最多分析.
解答 解:A.溶液酸碱性不影响水的离子积,则a点水的离子积Kw=1.0×10-14,故A正确;
B.b点呈酸性,溶液中一定满足电荷守恒:c(NH4+)+c(H+)=c(Cl-)+c(OH-),故B正确;
C.c点pH=7,则c(H+)=c(OH-),溶液中电荷守恒为c(NH4+)+c(H+)=c(Cl-)+c(OH-),则c(Cl-)=c(NH4+),即c(NH4+)=c(Cl-)>c(H-)=c(OH-),故C正确;
D.d点时盐酸和氨水恰好完全反应,放热最多,再加盐酸温度降低只能是加入盐酸的温度低于溶液温度,这才是温度下降的原因,故D错误;
故选D.
点评 本题考查了酸碱混合定性判断及溶液pH的计算,题目难度中等,明确滴定曲线中各点的pH是解答的关键,注意掌握物料守恒、电荷守恒的含义及应用方法,试题培养了学生的分析能力及灵活应用能力.


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源: 题型:选择题
| A. | 把浓硝酸放在棕色瓶中,并置于冷暗处保存 | |
| B. | 把Na保存在煤油中 | |
| C. | 把NaOH溶液放在带橡皮塞的玻璃瓶中 | |
| D. | 把氢氟酸放在玻璃瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
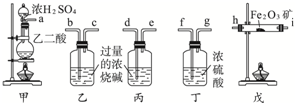
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 醋酸溶液与碳酸钙反应,缓慢放出二氧化碳 | |
| B. | 用醋酸溶液做导电性实验,灯泡很暗 | |
| C. | 0.1mol/L醋酸溶液可以使紫色石蕊试液变红 | |
| D. | 0.1 mol/L醋酸溶液的pH=3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②④ | C. | ③④ | D. | ①②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
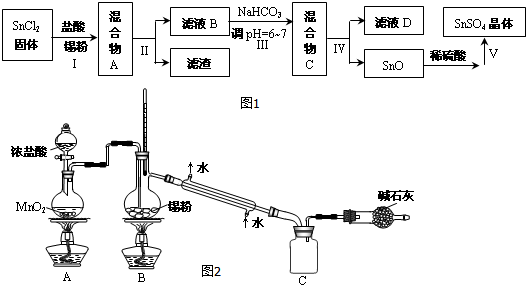
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com