
| 压强/MPa 转化率/% 温度/℃ | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
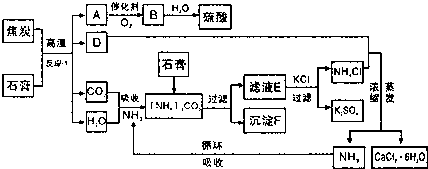
分析 工业上以磷肥生产形成的副产物石膏(CaSO4•2H2O)与焦炭为原料可生产硫酸,同时可以得到硫酸钾肥料和氯化钙水合物储热材料,依据流程图分析可知,生成硫酸的步骤中,A为SO2,B为SO3,CO2,H2O吸收氨气生成(NH4)2CO3,碳酸铵和石膏反应生成碳酸钙沉淀和硫酸铵溶液,沉淀F为CaCO3和CaSO4•2H2O,在硫酸铵溶液中加入氯化钾,利用物质溶解度分离得到硫酸钾和氯化铵,氯化铵和D反应生成氨气和氯化钙晶体,说明D为CaO,溶于水生成的氢氧化钙和氯化铵反应得到氯化钙溶液,浓缩蒸发得到CaCl2•6H2O.
解答 解:工业上以磷肥生产形成的副产物石膏(CaSO4•2H2O)与焦炭为原料可生产硫酸,同时可以得到硫酸钾肥料和氯化钙水合物储热材料,依据流程图分析可知,生成硫酸的步骤中,A为SO2,B为SO3,CO2,H2O吸收氨气生成(NH4)2CO3,碳酸铵和石膏反应生成碳酸钙沉淀和硫酸铵溶液,沉淀F为CaCO3和CaSO4•2H2O,在硫酸铵溶液中加入氯化钾,利用物质溶解度分离得到硫酸钾和氯化铵,氯化铵和D反应生成氨气和氯化钙晶体,说明D为CaO,溶于水生成的氢氧化钙和氯化铵反应得到氯化钙溶液,浓缩蒸发得到CaCl2•6H2O;
(1)分析判断反应Ⅰ是石膏和碳在高温下反应生成氧化钙,二氧化硫,二氧化碳,水,配平书写化学方程式为:CaSO4•2H2O+C$\frac{\underline{\;高温\;}}{\;}$2CaO+2SO2↑+CO2↑+4H2O↑;
故答案为:CaSO4•2H2O+C$\frac{\underline{\;高温\;}}{\;}$2CaO+2SO2↑+CO2↑+4H2O↑;
(2)沉淀F为CaCO3和CaSO4•2H2O,故答案为:CaCO3和CaSO4•2H2O;
(3)检验碳酸根离子的存在,可以取少量滤液加入盐酸,根据生成气体现象分析判断碳酸根离子的存在,实验方法为:取少许滤液滴加到盐酸中产生气泡;
故答案为:取少许滤液滴加到盐酸中产生气泡;
(4)氯化钙结晶水合物(CaCl2•6H2O)是目前常用的无机储热材料,是因为氯化钙结晶水合物熔点低易熔化,且无毒,与易溶于水,能导电无关;
故答案为:cd;
(5)依据图表数据分析可知,二氧化硫氧化为三氧化硫的反应是放热反应,温度低利于反应正向进行,但反应速率慢,增大压强对二氧化硫的转化率增加不大,所以为提高反应速率,在400°C-500°C,常压下,二氧化硫转化率较高,且在此温度下催化剂活性最大;
故答案为:常压、400-500℃、催化剂的条件下.
点评 本题考查了物质流程分析,反应产物的判断方法,依据化学平衡原理选择生产需要的合适条件,物质性质和反应过程是解题关键,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016-2017学年山西省高二上10月月考化学试卷(解析版) 题型:选择题
制造焊锡时,在金属铅中加入锡的主要原因是
A.增加强度 B.降低熔点
C.增加硬度 D.增强抗腐蚀能力
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一上期中化学试卷(解析版) 题型:选择题
如果你家里的食用花生油混有水份,你将采用下列何种方法分离
A.过滤 B.蒸馏 C.分液 D.萃取
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁沈阳东北育才学校高一阶段考一化学卷(解析版) 题型:选择题
某元素1个原子的质量是a g,又知1个12C原子的质量为b g,NA表示阿伏加德罗常数,则下列各式中能表示该原子的相对原子质量数值的是( )
①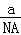 ②
②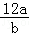 ③aNA ④
③aNA ④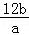
A.①② B.①④ C.②④ D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 标况下1molCCl4所占体积约为22.4L | |
| B. | 不同分散系其对应分散质的微粒直径不同 | |
| C. | 1molO2与1molO3所含的原子数目相等 | |
| D. | NaCl晶体和熔化的NaCl都属于电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al易导电,属于电解质 | |
| B. | BaSO4难溶于水,属于非电解质 | |
| C. | HCl的气体和液体都不导电,但HCl属于电解质 | |
| D. | SO2溶于水能导电,所以SO2是电解质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com