
【题目】(1)有一真空瓶质量为m1,该瓶充入空气后质量为m2。在相同状况下,若改为充入某气体A时,总质量为m3。已知空气相对分子质量为29,则A的相对分子质量是_______________
(2)把一定量铁粉放入氯化铁溶液中,完全反应后,得到溶液中Fe2+和Fe3+的浓度恰好相等。则已反应的Fe3+和未反应的Fe3+的物质的量之比为___________
(3)已知铜和稀硝酸反应方程式为3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,则被氧化的物质与被还原的物质质量比为___________
(4)A、B两个烧瓶中分别装80mL 3.0 mol/L的盐酸和NaOH溶液,再分别加等质量的铝粉,在相同状况下产生的气体的体积比为A:B=2:5,则加入铝粉的质量为___________
【答案】29(m3-m1)/(m2-m1) 2:3 32:21 5.4g
【解析】
根据阿伏加德罗定律进行计算;根据化学方程式进行过量判断及相关计算。
(1)充入气体A的质量为(m3-m1);相同条件下,等体积的气体质量之比等于相对分子质量之比,空气的平均相对分子质量为29,设A的相对分子质量是x,则![]() =
=![]() ,则x=29(m3-m1)/(m2-m1),
,则x=29(m3-m1)/(m2-m1),
故答案为:29(m3-m1)/(m2-m1);
(2)设已反应的Fe3+的物质的量为2mol,则:
Fe+2Fe3+=3Fe2+
2mol 3mol
溶液中Fe2+的物质的量为3mol,溶液中的Fe3+和Fe2+浓度相等,所以未反应的Fe3+的物质的量为3mol,则已反应的Fe3+和未反应的Fe3+的物质的量之比为2mol:3mol=2:3,
故答案为:2:3;
(3)3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O反应中,Cu化合价升高,被氧化,硝酸化合价降低,被还原,3molCu被氧化同时只有2mol硝酸被还原,所以被氧化的物质与被还原的物质质量比为![]() =32:21,
=32:21,
故答案为:32:21;
(4)盐酸和氢氧化钠钠的物质的量为:0.08L×3.0 mol/L=0.24mol,
根据2Al +6HCl = 2AlCl+ 3H↑, 2Al + 2H2O + 2NaOH = 2NaAlO2 + 3H2↑得加入等质量的铝粉,可见盐酸的量不足,则根据盐酸的物质的量算出氢气的物质的量为:n(H2)=0.24mol×1/2=0.12mol,相同条件下,气体体积之比等于物质的量之比,则铝与氢氧化钠反应放出的氢气物质的量为:n(H2)= 0.12mol×5/2=0.3mol,与氢氧化钠溶液反应时,铝完全反应,故n(Al)=2/3 n(H2)=2/3×0.3mol=0.2mol,m(Al)=0.2mol×27g/mol=5.4g,
故答案为:5.4g。


 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:
【题目】有关物质的转化关系如下图所示(部分物质和条件已略去)。A是由两种元素组成的难溶于水的物质,两种元素的质量比为7:4;B是强酸;C的摩尔质量为34g·mol-1; F是最常见的无色液体;无色气体G能使品红溶液褪色;向含有I的溶液中滴加KSCN溶液,溶液出现血红色。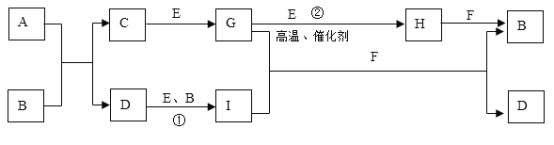
请回答下列问题:
(1)A的化学式____________________________。
(2)C的电子式____________________________。
(3)反应①的离子方程式_______________________________________________________。
(4)反应②的化学方程式_______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用如下装置制取氯气,并用氯气进行实验。回答下列问题:
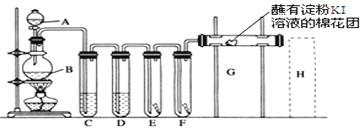
(1)A中盛有浓盐酸,B中盛有MnO2,写出反应的离子方程式___________________。
(2)D中放入浓H2SO4其目的是_____________________________。
(3)E中为红色干布条,F中为红色湿布条,可观察到的现象是___________,对比E和F中现象的差异可得出的结论是________________________________。
(4)G处的现象是____________________________________。
(5)用化学方程式写出H处尾气吸收装置中的反应原理____________。
(6)家庭中常用消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)清洁卫生。某品牌消毒液包装上说明如下图。

①消毒液与洁厕灵不能同时使用,原因是(用离子方程式表示)____________。
②需“密闭保存”的原因____________________________________________。
(7)工业上用亚氯酸钠和稀盐酸为原料制备 ClO2 ,写出反应的化学方程式____________。Cl2和ClO2都是强氧化剂,能杀死水中的病菌。等质量的ClO2的氧化能力是Cl2的_______倍。
(8)氰(CN)2、硫氰(SCN)2的化学性质和卤素(X2)很相似,化学上称为拟卤素,如:[(SCN)2+H2O = HSCN+HSCNO]。它们阴离子的还原性强弱为 Cl-<Br-<CN-<SCN-<I-。试写出:KBr和KSCN的混合溶液中加入(CN)2,反应的化学方程式为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】成环反应在有机合成中具有重要应用,某环状化合物G的合成过程如下:

(1)A→B为加成反应,则B的结构简式是______;B→C的反应类型是______.
(2)G中含有的官能团名称是______;F的化学式为______.
(3)D→E的化学方程式是___________________________________________.
(4)H是F的同分异构体,具有下列结构特征:①核磁共振氢谱除苯环吸收峰外仅有1个吸收峰;②存在甲氧基(CH3O—).H的结构简式是________________.
(5)由C通过加聚反应合成的高分子化合物M的化学方程式为______.
(6)下列说法正确的是______.
a.A能和HCl反应得到聚氯乙烯的单体
b.D和F中均含有2个π键
c.1mol G完全燃烧生成8mol H2O
d.F能发生加成反应、取代反应、氧化反应.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置。
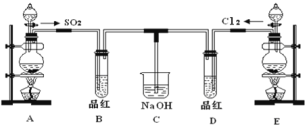
(1)实验室用装置E制备Cl2,其反应的离子方程式为__________________________;若有8mol的HCl参加反应,则转移的电子总数为________。
(2)该装置中氢氧化钠溶液的作用是___________________。
(3)通气后B、D两个试管中的现象______________。停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为B:________,D:________。
(4)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强。他们将制得的SO2和Cl2按1:1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用离子方程式表示)____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作中一定会产生误差的是
A.在中和热的测定实验中用Ba(OH)2代替NaOH,用H2SO4代替HCl
B.将pH试纸用蒸馏水润湿后测某溶液的pH
C.用碱石灰来干燥氨气
D.使用天平称量时误将药品与砝码的位置放反
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学是一门以实验为基础的学科,试回答以下问题:
I用质量分数为36.5%的浓盐酸(密度为1.16 g·cm-3)配制成1 mol·L-1的稀盐酸。现实验室仅需要这种盐酸220 mL,试回答下列问题:
(1)配制稀盐酸时,应选用容量为________mL的容量瓶。
(2)经计算需要________mL浓盐酸,在量取时宜选用下列量筒中的________。
A.5 mL B.10 mL C.25 mL D.50 mL
(3)在量取浓盐酸后,进行了下列操作:
①等稀释的盐酸的温度与室温一致后,沿玻璃棒注入250 mL容量瓶中。
②往容量瓶中小心加蒸馏水至液面离容量瓶刻度线1~2 cm时,改用胶头滴管加蒸馏水,使溶液的液面与瓶颈的刻度标线相切。
③在盛盐酸的烧杯中注入蒸馏水,并用玻璃棒搅动,使其混合均匀。
④用蒸馏水洗涤烧杯和玻璃棒2至3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是(填序号)____________。
(4)在上述配制过程中,用刚刚洗涤洁净的量筒来量取浓盐酸,其配制的稀盐酸浓度________(填“偏高”、“偏低”或“无影响”)。若未用蒸馏水洗涤烧杯内壁或未将洗涤液注入容量瓶,则配制的稀盐酸浓度是________(填“偏高”、“偏低”或“无影响”)。
II实验室用以下装置进行实验
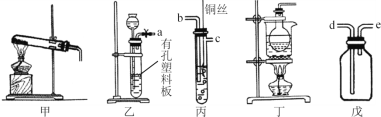
(5)装置甲和戊用于制取并收集少量氨气,甲中发生反应的化学方程式为: ______________________。 戊装置收集氨气应从收集装置的_____(填字母序号)导管进气。
(6)选用装置乙、丙、戊制备、收集一氧化氮气体,乙中塑料板上若放置石灰石,戊中 盛满稀NaOH溶液,仪器正确的连接顺序为________________________ (用接口字母表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是( )
A. 碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑
B. 将氯气溶于水制备次氯酸:Cl2+H2O =2H++Cl-+ClO-
C. 氢氧化钡溶液与稀H2SO4 反应:Ba2++SO42-=BaSO4↓
D. 氯化铜溶液与铁粉反应:Cu2++Fe=Fe2++Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把400mLNH4HCO3和Na2CO3的混合溶液分成两等份,取一份加入含a mol氢氧化钠的溶液恰好反应完全,另一份加入含b mol HCl的盐酸恰好反应完全,则该混合溶液中c(Na+)为
A. (b/10-a/20)mol/L B. (2b-a)mol/L C. (5b-5a/2)mol/L D. (10b-5a)mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com