
【题目】酶在生命活动和工业生产中都有很好的催化效果。有下列物质的转化关系:
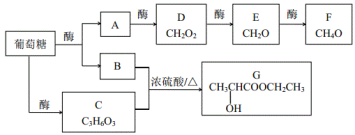
(1)E→F的反应类型____;有机物B、C都含有的官能团名称____。
(2)下列说法正确的是___。
A.可以用![]() 溶液鉴别物质B、C、D
溶液鉴别物质B、C、D
B.物质C和D均可以发生取代反应
C.质量相同的葡萄糖和E完全燃烧,葡萄糖耗氧量多
D.物质F一定条件可以转化为E,E也可以转化为D
【答案】加成反应 羟基 BD
【解析】
由G可知C为CH3CHOHCOOH,B为CH3CH2OH,由分子式可知F为CH3OH,E为HCHO,D为HCOOH,A应为CO2;
(1)E为HCHO,可与氢气发生加成反应生成CH3OH,B为CH3CH2OH,C为CH3CHOHCOOH,都含有羟基;
(2)A.甲醇易溶于水,甲酸、乳酸与氢氧化钠溶液反应,没有明显的现象,不能鉴别,故A错误;
B.C为CH3CHOHCOOH,含有羟基和羧基,D为HCOOH,含有羧基,都可发生取代反应,故B正确;
C.E为HCHO,与葡萄糖的最简式相同,则质量相同的葡萄糖和E完全燃烧,消耗的氧气一样多,故C错误;
D.F为CH3OH,可发生氧化反应生成甲醛,甲烷可被氧化生成甲酸,故D正确;
故答案为:BD。


科目:高中化学 来源: 题型:
【题目】将一定量的铁与100mL 18.5mol/L浓硫酸充分加热反应后,铁完全溶解,同时生成气体33.6L(已换算为标准状况下的体积)。将反应后的溶液稀释至1L,测得溶液的pH=1,并取少量溶液加入KSCN溶液无明显现象。(不考虑气体的溶解)
(1)反应中共消耗金属Fe的质量为________。
(2)将反应后的溶液稀释至1L时溶液中![]() 为________。
为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实可以用勒夏特列原理解释的是
A. 高锰酸钾溶液与草酸发生化学反应刚开始缓慢,随后反应迅速加快
B. 实验室采用排饱和食盐水的方法收集氯气(Cl2+H2O![]() HCl+HClO)
HCl+HClO)
C. 500 ℃左右的温度比室温更有利于合成氮反应N2(g)+ 3H2 (g)![]() 2NH3(g) △H<0
2NH3(g) △H<0
D. FeCl3+3KSCN![]() Fe(SCN)3+3KCl, 增大KCl的浓度则溶液的颜色变浅
Fe(SCN)3+3KCl, 增大KCl的浓度则溶液的颜色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烷是液化石油气主要成分之一,是一种优良的燃料。试回答下列问题:
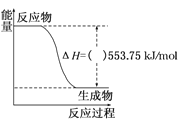
(1)如图是一定量丙烷完全燃烧生成CO2和1mol H2O(l)过程中的能量变化图,(图中的括号内填入“+”或“﹣”)_____。写出表示丙烷燃烧热的热化学方程式:_________________________
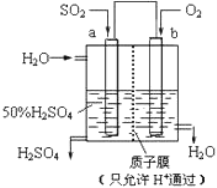
(2)科研人员设想用如图所示装置生产硫酸。
①上述生产硫酸的总反应方程式为_____________,b 是___________ 极(填“正”或“负”),b 电极反应式为______________________________,a 电极发生______________ (填“氧化反应”或“还原反应”)。②生产过程中H+向_____(填 a 或 b)电极区域运动。
(3)将两个铂电极插入氢氧化钾溶液中,向两极分别通入甲烷和氧气,可构成甲烷燃料电池,已知通入甲烷的一极为负极,其电极反应式为:_______________________。电池在放电过程中,溶液的pH值将______________ 。(填“下降”“上升”或“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水中溶氧量(DO)是衡量水体自净能力的一个指标,通常用每升水中溶解氧分子的质量表示,单位mg·L-1,我国《地表水环境质量标准》规定,生活饮用水源的DO不能低于5mg·L-1。某化学小组同学设计了下列装置(夹持装置略),测定某河水的DO。
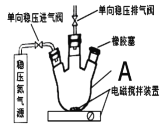
Ⅰ.测定原理:
碱性条件下,O2将Mn2+氧化为MnO(OH)2:①2Mn2++O2+4OH-=2MnO(OH)2↓,酸性条件下,MnO(OH)2将I-氧化为I2:②MnO(OH)2+I-+H+→Mn2++I2+H2O(未配平),用Na2S2O3标准溶液滴定生成的I2,③2S2O32-+I2=S4O62-+2I-
Ⅱ.测定步骤
a.安装装置,检验气密性,充N2排尽空气后,停止充N2。
b.向A中加入200mL水样
c.向A中依次迅速加入1mLMnSO4无氧溶液(过量),2mL碱性KI无氧溶液(过量),开启搅拌器,至反应①完全。
d.搅拌并向A中加入2mL硫酸无氧溶液至反应②完全,溶液为中性或弱酸性。
e.从A中取出40.00mL溶液,以淀粉作指示剂,用0.01000mol·L-1Na2S2O3溶液进行滴定,记录数据。
f.重复步骤e的操作2~3次
g.处理数据(忽略氧气从水样中的溢出量和加入试剂后水样体积的变化)。
回答下列问题:
(1)仪器A的名称为___。
(2)配置以上无氧溶液时,除去所用溶剂水中氧的简单操作为___。
(3)配平反应②的方程式。___MnO(OH)2+___I-+___H+→___Mn2++___I2+___H2O
(4)步骤e中达到滴定终点的现象为___。
(5)若某次滴定消耗Na2S2O3溶液4.50mL,水样的DO=___mg/L(保留一位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应:2A(s) ![]() B(g)+C(g),在一定条件下的刚性密闭容器中,起始时加入一定量的A,能判断反应达到平衡状态的有( )
B(g)+C(g),在一定条件下的刚性密闭容器中,起始时加入一定量的A,能判断反应达到平衡状态的有( )
①单位时间内生成2molA的同时生成1molB ②v (B): v (C)=1:1 ③密闭容器中混合气体的平均摩尔质量不变 ④混合气体的密度不再改变 ⑤B的体积分数不再改变 ⑥混合气体的压强不再改变
A. 3个 B. 4个 C. 5个 D. 6个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种可充电锂-空气电池如图所示。当电池放电时,O2与Li+在多孔碳材料电极处生成Li2O2-x、(x=0或1),下列说法正确的是

A. 多孔碳材料电极为负极
B. 外电路电子由多孔碳材料电极流向锂电极
C. Li+向多孔碳材料区迁移
D. x=0时,正极反应式为:2Li++O2+4e-=Li2O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用不同方法制得白色的Fe(OH)2沉淀。
(1)用未被氧化的FeSO4溶液与煮沸过的蒸馏水配制的NaOH溶液反应制备,制备过程中下列说法正确的是_______
A.用硫酸亚铁晶体配制上述FeSO4溶液时还需加入适量盐酸防止水解
B.除去蒸馏水中溶解的O2也可以采取振摇、静止的方法
C.生成白色Fe(OH)2沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液
D.FeSO4溶液上面加一层苯可以防止空气中氧气直接与溶液接触
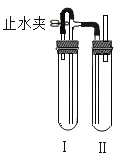
(2)在如图装置中,用NaOH溶液、铁屑、稀H2SO4等试剂制备。在试管I 里加入稀H2SO4和铁屑,在试管II里加入NaOH溶液,打开止水夹,塞紧塞子,检验试管Ⅱ出口处排出的氢气的纯度。当排出的H2纯浄时,再____(填操作步骤),这样一段时间后试管Ⅲ中制得的Fe(OH)2沉淀能较长时间保持白色,其理由是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是由短周期元素组成的一些单质及其化合物之间的转化关系图。常温常压下,D、F、K均为无色无刺激性气味的气体,B是最常见的无色液体,A是由单质C在D中燃烧生成的淡黄色固体。(反应中生成的部分物质已略去)
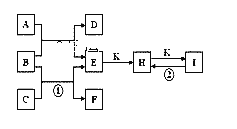
请回答下列问题:
(1)物质A的化学式为________;物质D的名称________;
(2)化合物I的化学式为_____________________;
(3)反应①的化学方程式为_______________________________________;
反应②的化学方程式为_______________________________________;
A与B反应的化学方程式________________________________________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com