
分析 (1)依据配制一定物质的量浓度溶液的一般步骤选择需要的仪器;
(2)分析操作对溶质的物质的量n和溶液的体积V的影响,依据C=$\frac{n}{V}$可知,当操作使溶质的物质的量n偏大或者使溶液体积V偏小,都会使溶液浓度偏高,反之溶液浓度偏低.
解答 解:(1)配制一定物质的量浓度溶液的一般步骤:计算、称量、溶解、移液、洗涤、定容,用到的仪器:
托盘天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管,所以还缺少的仪器:药匙、玻璃棒、500mL容量瓶、胶头滴管;
故答案为:药匙、玻璃棒、500mL容量瓶、胶头滴管;
(2)A.称量时使用了生锈的砝码,导致称取的溶质的质量偏大,溶质的物质的量偏大,溶液浓度偏高;
B.将NaOH放在纸张上称量,导致称取的溶质的物质的量偏小,溶液浓度偏低;
C.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中,冷却后,溶液体积偏小,溶液浓度偏高;
D.往容量瓶中移液时,有少量液体溅出,导致溶质的物质的量偏小,溶液浓度偏低;
E.未洗涤溶解NaOH的烧杯,导致溶质的物质的量偏小,溶液浓度偏低;
F.定容时仰视刻度线,导致溶液体积偏大,溶液浓度偏低;
G.容量瓶未干燥即用来配制溶液,对溶质的物质的量和溶液体积都不会产生影响,溶液浓度不受影响;
H.定容后盖上瓶塞反复摇匀,静置后,发现液面不到刻度线,再加水至刻度线,导致溶液体积偏大,溶液浓度偏低;
所以:偏大的有AC;
偏小的有BDEFH;
无影响的有G;
故答案为:AC;BDEFH;G.
点评 本题考查了一定物质的量浓度溶液的配制,明确配制原理和操作步骤是解题关键,注意误差分析的方法,题目难度不大.


 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案科目:高中化学 来源: 题型:选择题
| A. | ①④⑤⑦ | B. | ③⑥⑦ | C. | ④⑤⑥ | D. | ①②③⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 肯定有Al3+、Mg2+、NO3-,可能有NH4+、K+ | |
| B. | 肯定有Al3+、K+、Cl-,肯定没有MnO4-、Mg2+ | |
| C. | 肯定有Al3+、NH4+、Cl-、NO3-,一定没有HCO3-、Mg2+、MnO4- | |
| D. | 该溶液可能显弱酸性,也可能显中性 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 3mol A、2mol B | 6mol A、4mol B | 2mol C |
| 到达平衡的时间(min) | 5 | 8 | |
| A的浓度(mol/L) | c1 | c2 | |
| C的体积分数 | w1 | w3 | |
| 混合气体密度(g/L) | ρ1 | ρ2 |
| A. | 若x<4,则2c1>c2 | |
| B. | 若x=4,则w3=w1 | |
| C. | 无论x的值是多少,均有2ρ1=ρ2 | |
| D. | 容器甲达到平衡所需的时间比容器乙达到平衡所需的时间短 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
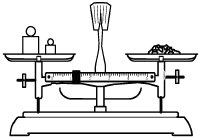 | 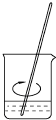 | 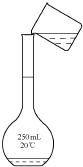 | 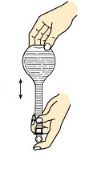 |
| A.称量 | B.溶解 | C.转移 | D.摇匀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时若1 mL pH=1的盐酸与100 mL 氨水溶液混合后,溶液的pH=7,则氨水溶液的pH=11 | |
| B. | 将0.2 mol•L-1盐酸与0.1 mol•L-1的KAlO2溶液等体积混合,溶液中离子浓度由小到大的顺序:c(OH-)<c(H+)<c(Al3+)<c(K+)<c(Cl-) | |
| C. | pH相等的①NH4Cl ②(NH4)2SO4 ③NH4HSO4溶液:c(NH4+)大小顺序为②>①>③ | |
| D. | 0.1mol/LNaHCO3溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中:c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/LCH3COONa与0.1mol/LHCl溶液等体积混合:c(Na+)=c(Cl-)>c(CH3COO-)>c(OH-) | |
| B. | 0.1mol/LNH4Cl与0.1mol/L氨水溶液等体积混合:c(NH3•H2O)>c(NH4+)>c(Cl-)>c(OH-) | |
| C. | 0.1mol/LNa2CO3与0.1mol/LNaHCO3溶液等体积混合:2c(Na+)=3c(CO32-)+3c(HCO3-)+3c(H2CO3) | |
| D. | Na2C2O4溶液与HCl溶液等体积混合(H2C2O4是二元弱酸):2c(C2O42-)+c(HC2O4-)+c(OH-)+c(Cl-)=c(Na+)+c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
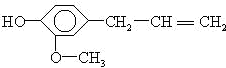 据此结构分析,下列说法正确的是( )
据此结构分析,下列说法正确的是( )| A. | 可以燃烧,只能与溴水发生加成反应 | |
| B. | 可与NaOH溶液反应,也可与FeCl3溶液反应 | |
| C. | 不能与金属钠反应放出H2 | |
| D. | 可以与小苏打溶液反应放出CO2气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com