
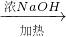 得到使湿润蓝色石蕊试纸变红色的气体,说明样品中含NH4+
得到使湿润蓝色石蕊试纸变红色的气体,说明样品中含NH4+ 无明显现象
无明显现象 出现白色沉淀,说明样品中含SO42-
出现白色沉淀,说明样品中含SO42- 出现白色沉淀,说明样品中含Ag+
出现白色沉淀,说明样品中含Ag+ 得到使澄清石灰水变浑浊的气体,说明样品中含CO32-或HCO3-
得到使澄清石灰水变浑浊的气体,说明样品中含CO32-或HCO3-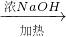 得到使湿润红色石蕊试纸变蓝色的气体,说明样品中含NH4+,故A错误;
得到使湿润红色石蕊试纸变蓝色的气体,说明样品中含NH4+,故A错误; 出现白色沉淀,说明样品中含Ag+或是含有硅酸根离子,氯化银和硅酸均为白色沉淀,故C错误;
出现白色沉淀,说明样品中含Ag+或是含有硅酸根离子,氯化银和硅酸均为白色沉淀,故C错误; 得到使澄清石灰水变浑浊的气体,说明样品中含SO32-、CO32-或HCO3-,故D错误.
得到使澄清石灰水变浑浊的气体,说明样品中含SO32-、CO32-或HCO3-,故D错误.

科目:高中化学 来源: 题型:阅读理解
| 实验操作 | 实验现象 | |
| 步骤1 | 在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水,充分反应,过滤,将滤液分为若干份. | 有少量气泡产生,溶液的黄绿色褪去. |
| 步骤2 | 将第一份滤液与稀盐酸混合. | 产生大量气泡. |
| 步骤3 | 将第二份滤液加热. | 溶液变浑浊,且有大量无色气体产生. |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验操作 | 实验现象 | |
| 步骤1 | 在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水,充分反应,过滤,将滤液分为若干份 | 有少量气泡产生,溶液的黄绿色褪去 |
| 步骤2 | 将第一份滤液与稀盐酸混合 | 产生大量气泡 |
| 步骤3 | 将第二份滤液加热 | 溶液变浑浊,且有大量无色气体产生 |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组利用饱和氯水与石灰石的反应,制取较浓的HClO溶液,并对所得溶液中的部分阴离子进行检验。
| 实验操作 | 实验现象 | |
| 步骤1 | 在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水,充分反应,过滤,将滤液分为若干份 | 有少量气泡产生,溶液的黄绿色褪去 |
| 步骤2 | 将第一份滤液与稀盐酸混合 | 产生大量气泡 |
| 步骤3 | 将第二份滤液加热 | 溶液变浑浊,且有大量无色气体产生 |
⑴步骤1过滤的目的是__________________________________________。
⑵步骤2、步骤3的实验目的都是 ;为达到该实验目的,还可以采取的方法是 。
⑶请你设计一个简单的实验方案,证明步骤1所得滤液中的HClO浓度比饱和氯水中HClO浓度大: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com