
在微生物作用的条件下,NH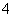 经过两步反应被氧化成NO
经过两步反应被氧化成NO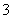 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:
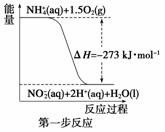
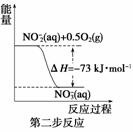
①第一步反应是________反应(选填“放热”或“吸热”),判断依据是________________________________________________________________________。
②1 mol NH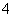 (aq)全部氧化成NO
(aq)全部氧化成NO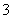 (aq)的热化学方程式是________________________________________________________________________。
(aq)的热化学方程式是________________________________________________________________________。
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案科目:高中化学 来源: 题型:
体积相同的盐酸和醋酸两种溶液,n(Cl-)=n(CH3COO-)=0.01 mol,下列叙述错误的是( )
A.它们与NaOH完全中和时,醋酸溶液所消耗的NaOH多
B.它们分别与足量CaCO3反应时,放出的CO2一样多
C.两种溶液的pH相同
D.分别用水稀释相同倍数时,n(Cl-)<n(CH3COO-)
B。CH3COOH属于弱酸,体积相同的两种溶液中,由n(Cl-)=
查看答案和解析>>
科目:高中化学 来源: 题型:
已知HClO是比H2CO3还弱的酸,氯水中存在下列平衡:Cl2+H2O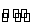 HCl
HCl
+HClO;HClO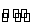 H++ClO-,达平衡后:
H++ClO-,达平衡后:
(1)要使HClO的浓度增加,可加入下列物质(填代号)________。
A.SO2 B.CaCO3 C.HCl D.NaOH
(2)由此说明在实验室里可用排饱和食盐水收集Cl2的理由是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某反应过程能量变化如图所示,下列说法正确的是(双选)( )
A.反应过程a有催化剂参与
B.该反应为放热反应,热效应等于ΔH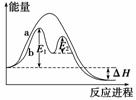
C.改变催化剂,可改变该反应的活化能
D.有催化剂的条件下,反应的活化能等于E1+E2
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,在水溶液中1 mol Cl-、ClO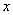 (x=1,2,3,4)的能量(kJ)相对大小如图所示。
(x=1,2,3,4)的能量(kJ)相对大小如图所示。
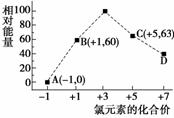
①D是________(填离子符号)。
②B—→A+C反应的热化学方程式为______________________(用离子符号表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
依据事实,写出下列反应的热化学方程式。
(1)适量的N2和O2完全反应,每生成23 g NO2吸收16.95 kJ热量。N2与O2反应的热化学方程式为______________________________。
(2)18 g葡萄糖与适量O2反应,生成CO2和液态水,放出280.4 kJ热量。葡萄糖燃烧的化学方程式为______________________________。
(3)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态H2O。已知室温下2 g SiH4自燃放出热量89.2 kJ。SiH4自燃的热化学方程式为________________________________。
(4)下图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:____________________________________________。
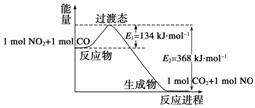
(5)直接排放煤燃烧产生的烟气会引起严重的环境问题。煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
CH4(g)+2NO2(g)===N2(g)+CO2(g)+2H2O(g)
ΔH1=-867 kJ·mol-1①
2NO2(g)N2O4(g) ΔH2=-56.9 kJ·mol-1②
写出CH4(g)催化还原N2O4(g)生成N2(g)和H2O(g)的热化学方程式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关阿伏加德罗常数(NA)的说法错误的是 ( )
| A. | 常温常压下28克N2所含的原子数目为2NA | |
|
| B. | 标准状况下0.5molH2O含有的原子数目为1.5NA |
|
| C. | 任何条件下0.5mol氨气分子的分子数一定是0.5NA |
|
| D. | 49克H2SO4中含有的原子数目为1.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
乙炔是有机合成工业的一种重要原料。工业上曾用CaC2与水反应生成乙炔。
⑴CaC2中C22-与O22+互为等电子体,O22+的电子式可表示为 ,1mol O22+中含有的π键数目为 。
⑵将乙炔通入[Cu(NH3)2]Cl溶液中生成红棕色沉淀Cu2C2。Cu+简写的核外电子排布式为 。
⑶乙炔与HCN反应可得到丙烯腈(CH2=CH—C≡N), 丙烯腈分子中碳原子轨道的杂化类型是 ;分子中处于同一直线上原子数目最多有 个。
⑷CaC2晶体的晶胞结构与NaCl晶体相似(如图所示),但CaC2晶体中哑铃形的C22-的存在,使晶胞沿一个方向拉长, CaC2晶体中一个Ca2+周围距离最近的C22-数目为 。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com