
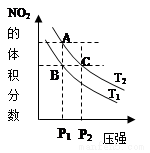
 ��ӦN2O4��g��?2NO2��g����H=+57kJ•mol-1�����¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ��ʾ������˵����ȷ���ǣ�������
��ӦN2O4��g��?2NO2��g����H=+57kJ•mol-1�����¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ��ʾ������˵����ȷ���ǣ�������| A�� | �����º���ʱ���������ƽ�����淴Ӧ�����ƶ� | |
| B�� | A��C�����������ɫ��A�Cdz | |
| C�� | ��״̬B��״̬A�������ü��ȵķ��� | |
| D�� | ��ΪB��C����NO2�����������ͬ�����Ի�ѧƽ�ⳣ��KB=KC�� |
���� N2O4��g��?2NO2��g����H=+57kJ•mol-1���÷�ӦΪ���ȷ�Ӧ���������¶ȣ���ѧƽ�����������ƶ������������NO2��������������������ѹǿ����ѧƽ�����������ƶ������������NO2�����������С��Ȼ����ͼ�����������
��� �⣺A�������º���ʱ�����������Ȼѹǿ�����μӷ�Ӧ�������Ũ�Ȳ��䣬ƽ�ⲻ�ƶ�����A����
B����ͬ�¶��£�����ѹǿ��ƽ�����淴Ӧ�����ƶ�����ƽ��ʱ��������Ũ�ȴ���ԭ��Ũ�ȣ�����Adz��C���B����
C����ͬѹǿ�£������¶ȣ�ƽ�������ƶ�����NO2�������������C��ȷ��
D����ѧƽ�ⳣ��ֻ���¶��йأ��¶Ȳ�ͬ����ƽ�ⳣ����ͬ�������¶ȣ�ƽ��������Ӧ�����ƶ�������������ĺ������������¶�T2��T1���¶�Խ�ߣ�����������ʵ���Խ��������ƽ�ⳣ��Խ����B��C�����ƽ�ⳣ����B��C����D����
��ѡC��
���� ���⿼����ͼ�������Ϊ��Ƶ���㣬���ݷ���ʽ�ص�ȷ���¶ȴ�С��ע��ƽ�ⳣ��ֻ���¶��йأ�������Ũ�ȡ�ѹǿ���أ��״�����B��ע��÷�Ӧͨ���ı�������ı�ѹǿ����Ȼƽ�����淴Ӧ�����ƶ�������������Ũ����Ȼ����Ϊ�״��㣮


 �¿α�����Ķ�ѵ��ϵ�д�
�¿α�����Ķ�ѵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
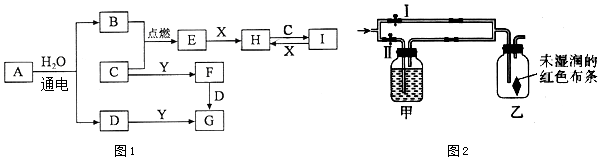
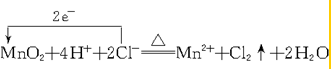 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���³�ѹ�£�22.4LH2O�к��е���ԭ����Ϊ2NA | |
| B�� | 17gNH3��18 g H2O�����е�������Ϊ10NA | |
| C�� | 2.7 g Al��������NaOH��Һ��Ӧ������H2�ķ�����Ϊ0.1NA | |
| D�� | 1 mol HCl�����еķ�������2L 0.5 mol/L�����е�������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���� | B�� | ʯ��ʯ | C�� | ʯӢ | D�� | ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Al2O3 | B�� | Fe | C�� | Al | D�� | ��NH4��2CO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1mol/L��CH3COOH��Һ��0.1mol/L��CH3COOH��Һ��ˮ�ĵ���̶�ǰ�ߴ��ں��� | |
| B�� | pH=2��HA��Һ��pH=12��NaOH��Һ�������Ϻ���Һ�Լ��ԣ����Ϻ����Һ�д���ƽ�⣺A-+H2O?HA+OH- | |
| C�� | ��֪ͬŨ�ȵ�NaA��NaB��NaX��Һ��������ǿ����Ks��HA����Ks��HB����Ks��HX�� | |
| D�� | ��֪������AgCl��Ksp=1.56��10-10����Ũ�Ⱦ�Ϊ2.2��10-5mol/L��AgNO3��Һ��NaCl��Һ�������ϣ������AgCl��ɫ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
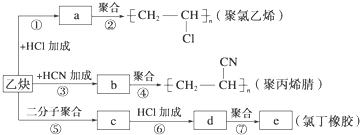
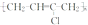 ����
����
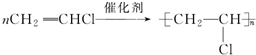 ��
�� ��
��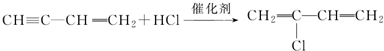 ��
��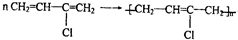 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2Na218O2+2CO2�T2Na2Cl8O3+O2 | |
| B�� | NH4Cl+2H2O?NH3•H2O+HCl | |
| C�� | K37ClO3+6HCl�TK37Cl+3Cl2��+3H2O | |
| D�� | 2KMnO4+5H218O2+3H2SO4�TK2SO4+2MnSO4+518O2��+8H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
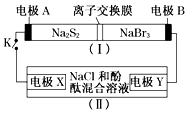 ��ͼ��ʾ��װ�ã�����һ�ֿɳ���ص�ʾ��ͼ��װ�ã���Ϊ���ص�ʾ��ͼ��װ�ã������ӽ���Ĥֻ����Na+ͨ������س䡢�ŵ�Ļ�ѧ����ʽΪ��2Na2S2+NaBr3$?_{���}^{�ŵ�}$Na2S4+3NaBr�����պ�Kʱ��X��������Һ�ȱ��ɫ������˵����ȷ���ǣ�������
��ͼ��ʾ��װ�ã�����һ�ֿɳ���ص�ʾ��ͼ��װ�ã���Ϊ���ص�ʾ��ͼ��װ�ã������ӽ���Ĥֻ����Na+ͨ������س䡢�ŵ�Ļ�ѧ����ʽΪ��2Na2S2+NaBr3$?_{���}^{�ŵ�}$Na2S4+3NaBr�����պ�Kʱ��X��������Һ�ȱ��ɫ������˵����ȷ���ǣ�������| A�� | װ�ã�����Na+������ͨ�����ӽ���Ĥ | |
| B�� | A�缫�ĵ缫��ӦʽΪNaBr3+2Na++2e-�T3NaBr | |
| C�� | X�缫�ĵ缫��ӦʽΪ2Cl--2e-�TCl2�� | |
| D�� | ÿ��0.1 mol Na+ͨ�����ӽ���Ĥ��X�缫�Ͼ�������״���µ�����1.12 L |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com