
对反应 4NH3 + 5O2 = 4NO + 6H2O,下列反应速率的最快的是
A. v(NH3)=0.25 mol·L-1·min-1 B. v(O2)=0.35mol·L-1·min-1
C. v(NO)=0.01 mol·L-1·S-1 D. v(H2O)=0.3 mol·L-1·min-1
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案科目:高中化学 来源: 题型:
完成下列反应的离子方程式:
(1)Ba(OH)2溶液与(NH4)2SO4溶液混合:____________________________________。
(2)CuSO4溶液与Ba(OH)2溶液混合:_______________________________________。
(3)NH4HCO3与过量NaOH溶液混合:______________________________________。
(4)Ba(OH)2与H2SO4两稀溶液混合:_______________________________________。
(5)Fe2O3溶于HI溶液中:________________________________________________。
(6)FeBr2溶液中通入过量Cl2:____________________________________________。
(7)FeO溶于稀HNO3中:_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知A物质的分子结构如下: , , 1 mol A与足量的
NaOH溶液混合共热,充分反应后最多消耗NaOH的物质的量为
A.6mol B.7mol C.8mo1 D.9mo1
查看答案和解析>>
科目:高中化学 来源: 题型:
离子液体是一种室温熔融盐,为非水体系,由有机阳离子、Al2Cl7—和AlCl4—组成的离子液体作电解液时,可在钢制品上电镀铝。
(1)钢制品应接电源的 极,已知电镀过程中不产生其他离子且有机阳离子不参与电极反应,阴极电极反应式为 。若改用AlCl3水溶液作电解液,则阴极产物为 。
(2)为测定镀层厚度,用NaOH溶液溶解钢制品表面的铝镀层,当反应转移6 mol电子时,所得还原产物的物质的量为 mol。
(3)用铝粉和Fe2O3做铝热反应实验,需要的试剂还有 。
a.KCl b. KClO3 c. MnO2 d. Mg
取少量铝热反应所得到的固体混合物,将其溶于足量稀H2SO4,滴加KSCN溶液无明显现象, (填“能”或“不能”)说明固体混合物中无Fe2O3,理由是 (用离子方程式说明)。
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示,是由碳棒、铁片和氯化铜溶液组成的原电池,下列叙述正确的是
 A.碳棒为正极
A.碳棒为正极
B.碳棒上的电极反应式为2H2O + O2 + 4e- = 4OH—
C.铁片上的电极反应式为2Cl——2e- = Cl2↑
D.铁片为阴极
查看答案和解析>>
科目:高中化学 来源: 题型:
有X、Y两种元素,原子序数≤20,X的原子半径小于Y,且X、Y原子的最外层电子数相同(选项中m、n均为正整数)。下列说法正确的是
A.若X(OH)n为强碱,则Y(OH)n也一定为强碱
B.若HnXOm为强酸,则X的氢化物溶于水一定显酸性
C.若X元素为非金属元素,则Y元素也一定为非金属元素
D.若Y的最高正价为+m,则X的最高正价一定为+m
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.非金属原子间不可能形成离子键
B.只有不同的原子间才能形成共价键
C.共价化合物中不可能含离子键
D.离子化合物中可能含有共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡: NH2COONH4(s) 2NH3(g)+CO2(g);不能判断该分解反应已经达到平衡的是:( )
2NH3(g)+CO2(g);不能判断该分解反应已经达到平衡的是:( )
A.密闭容器中氨气的浓度不变 B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变 D.2v(NH3)=v(CO2)
查看答案和解析>>
科目:高中化学 来源: 题型:
 可经三步反应制取
可经三步反应制取 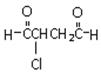 ,发生反应的类型依次是
,发生反应的类型依次是
A.水解反应、加成反应、氧化反应 B.加成反应、水解反应、氧化反应
C.水解反应、氧化反应、加成反应 D.加成反应、氧化反应、水解反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com