
| A. | ①④⑤ | B. | ②⑤⑥⑧ | C. | ②③⑥⑧ | D. | ⑤⑥⑦ |
分析 灼烧硫酸铜晶体制取无水硫酸铜所需用的仪器有灼烧药品的仪器坩埚、夹取坩埚的仪器坩埚钳,放置坩埚的三脚架、泥三角,搅拌药品的玻璃棒、冷却坩埚的仪器干燥器、加热的仪器酒精灯,据此分析解答.
解答 解:灼烧硫酸铜晶体制取无水硫酸铜所需用的仪器有灼烧药品的仪器坩埚、夹取坩埚的仪器坩埚钳,放置坩埚的三脚架、泥三角,搅拌药品的玻璃棒、冷却坩埚的仪器干燥器、加热的仪器酒精灯,所以需要的仪器有酒精灯、三脚架、泥三角、坩埚、坩埚钳、玻璃棒、干燥器,
故选B.
点评 本题以结晶水测定,为高频考点,明确仪器用途是解本题关键,侧重考查学生对仪器用途的了解及实验操作规范性,根据实验目的及仪器“从下而上”选取仪器,注意:加热坩埚应该放置在干燥器中干燥,而不是放置在空气中干燥,为易错点.


 全程金卷系列答案
全程金卷系列答案科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 溶解性 | |
| 环己醇 | 100 | 0.961 8 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.810 2 | 83 | 难溶于水 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①和② | B. | ①和③ | C. | ②和③ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
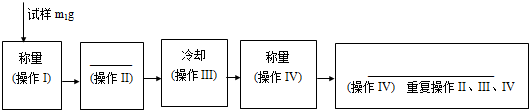
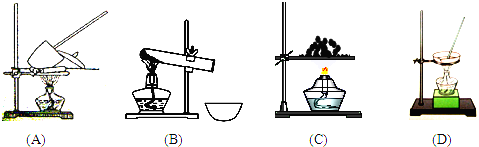
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
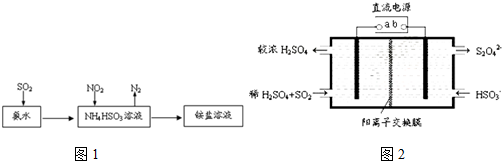
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
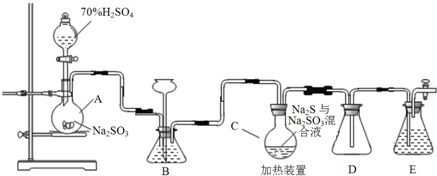
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增大压强,化学平衡不一定发生移动 | |
| B. | 通入与反应无关的氦气,化学平衡不发生移动 | |
| C. | 增大X或Y的物质的量,化学平衡一定发生移动 | |
| D. | 其它条件不变,升高温度,化学平衡一定发生移动 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com