
固体单质A和气体单质B在容积一定的密闭容器中完全反应生成气体C,同温下测得容器内压强不变,且反应后气体C的密度是原气体密度的4倍.则下列判断正确的是()
A. 两种单质的摩尔质量比为1:4
B. 生成物C中A的质量分数为75%
C. 生成物C中A、B的原子个数比为3:1
D. 反应前后气体分子数比为1:4
考点: 阿伏加德罗定律及推论.
专题: 阿伏加德罗常数和阿伏加德罗定律.
分析: 化学反应遵循质量守恒定律,同温下测得容器内压强不变,则气体的物质的量不变,反应后气体C的密度是原气体密度的4倍,则生成C的质量为B的质量的4倍,固体单质A的质量是体单质B的3倍,以此解答该题.
解答: 解:化学反应遵循质量守恒定律,反应前后的质量相等,同温下测得容器内压强不变,气体的物质的量不变,反应前后气体分子数比为1:1,
由密度变化知固体单质A的质量是气体单质B的3倍,即生成物C中A的质量分数为75%,由于A、B单质的组成不定,不能获得原子之间的比例.
故选B.
点评: 本题考查阿伏加德罗定律定律及其推论,题目难度中等,注意从质量守恒的角度判断,注意题中同温下测得容器内压强不变的条件.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
X、Y、Z、W四种物质的转化关系.下列组合中不符合该关系的是()
A B C D
X HCl Na2O2 Na2CO3 SO2
Y FeCl2 NaOH CO2 Na2SO3
Z Cl2 Na2CO3 Ca2CO3 H2SO4
W FeCl3 NaHCO3 Ca(HCO3)2 NaHSO3

A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
有一澄清透明的溶液,只可能含有大量的Fe3+、Fe2+、H+、AlO2﹣、Al3+、CO32﹣、NO3﹣七种离子中的几种,向该溶液中逐滴加入一定量1mol/L NaOH溶液的过程中,开始没有沉淀,而后才有沉淀.则下列判断正确的是()
A. 溶液中可能含有AlO2﹣
B. 溶液中可能含有NO3﹣
C. 溶液中一定不含Fe2+和Fe3+
D. 溶液中可能含有Fe3+,但一定不含Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
某强酸性溶液X含有Ba2+、Al3+、NH4+、Fe2+、Fe3+、CO32﹣、SO32﹣、SO42﹣、Cl﹣、NO3﹣中的一种或几种,取该溶液进行实验,实验内容如下:
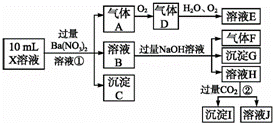
根据以上信息,回答下列问题:
(1)溶液X中除H+外还肯定含有的离子是 ﹣;不能确定是否含有的离子是 ,若要确定其中阳离子的存在,最可靠的化学方法是 +.
(2)沉淀G的化学式为
(3)写出有关离子方程式:步骤①中生成A .步骤②生成沉淀I ﹣.
(4)假设测定A、F、I均为0.01mol,10mL X溶液中n(H+)=0.04mol,当沉淀C物质的量(填:“<”或“=”或“>”某个值) 0.7(或<0.7) mol,表明不能确定是否含有的离子中一定存在 .(若不止一种可能,填一种情况即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A. 滴定管装滴定液时应先用滴定液润洗
B. 在50mL量筒中配制0.1000mol•L﹣1碳酸钠溶液
C. 用pH=1的盐酸配制100mLpH=2的盐酸需要100mL容量瓶、烧杯、玻璃棒、胶头滴管
D. 欲配制1.00L1.00mol•L﹣1的NaCl溶液,可将58.5gNaCl溶于1.00L水中
查看答案和解析>>
科目:高中化学 来源: 题型:
保护环境是每一个公民的责任,下列做法有利于保护环境的是( )
①推广使用无磷洗涤剂 ②城市生活垃圾分类处理 ③推广使用一次性木质筷子 ④推广使用清洁能源 ⑤过量使用化肥、农药 ⑥推广使用无氟冰箱.
A. ①②④⑤ B. ②③④⑥ C. ①②④⑥ D. ③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质属于同系物的是( )
A. CH3CH2CH2OH与CH3OH B. 
C. 乙酸与HCOOCH3 D. CH3CH2Cl与CH3CH2CH2Br
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com