
 实验室中利用含银废料(主要含有AgNO3和AgCl)制取硝酸银的实验步骤如下:
实验室中利用含银废料(主要含有AgNO3和AgCl)制取硝酸银的实验步骤如下:分析 (1)步骤1中向硝酸银中继续加NaCl溶液看是否有沉淀,可判断所加氯化钠是否足量;
(2)根据元素守恒和电荷守恒可书写步骤2中的离子方程式;
(3)步骤2中所得灰白色沉淀主要含有Ag、Al(OH)3和少量仍未反应的AgCl,可向沉淀中加入足量稀盐酸,充分反应后,过滤,洗涤沉淀,向沉淀中加入足量稀硝酸,充分反应后,过滤,将所得滤液蒸发浓缩、冷却结晶,过滤、洗涤、干燥,可得硝酸银固体;
(4)①配制100mL一定物质的量浓度的溶液,所需要的玻璃离仪器有烧杯、玻璃棒、100mL容量瓶、胶头滴管;
②用 NH4SCN标准溶液滴定硝酸银溶液,滴定终点时,SCN-与铁离子结合生成血红色溶液,据此判断;
③NH4SCN标准溶液的平均体积为29.00mL,则NH4SCN的物质的量为0.1000mol•L-1×0.029L=2.9×10-3 mol,根据Ag++SCN-=AgSCN↓可求得硝酸银的质量,进而确定质量分数;
解答 解:(1)步骤1中向硝酸银中继续加NaCl溶液看是否有沉淀,可判断所加氯化钠是否足量,实验步骤为静置,向上层清液中继续滴加NaCl溶液,若溶液不变浑浊,则NaCl已足量,
故答案为:静置,向上层清液中继续滴加NaCl溶液,若溶液不变浑浊,则NaCl已足量;
(2)步骤2加热时还产生能使澄清石灰水变浑浊的气体为二氧化碳,步骤2中的离子方程式为2Al+6AgCl+3CO3 2-+3H2O=2Al(OH)3+6Ag+6Cl-+3CO2↑,
故答案为:2Al+6AgCl+3CO3 2-+3H2O=2Al(OH)3+6Ag+6Cl-+3CO2↑;
(3)步骤2中所得灰白色沉淀主要含有Ag、Al(OH)3和少量仍未反应的AgCl,可向沉淀中加入足量稀盐酸,充分反应后,过滤,洗涤沉淀,向沉淀中加入足量稀硝酸,充分反应后,过滤,将所得滤液蒸发浓缩、冷却结晶,过滤、洗涤、干燥,可得硝酸银固体,
故答案为:加入足量稀盐酸,充分反应后,过滤;洗涤沉淀,向沉淀中加入足量稀硝酸,充分反应后,过滤;将所得滤液蒸发浓缩、冷却结晶,过滤;用冰水洗涤、干燥;
(4)①配制100mL一定物质的量浓度的溶液,所需要的玻璃离仪器有烧杯、玻璃棒、100mL容量瓶、胶头滴管,
故答案为:100mL容量瓶、胶头滴管;
②用 NH4SCN标准溶液滴定硝酸银溶液,滴定终点时,SCN-与铁离子结合生成血红色溶液,所以滴定终点的实验现象为溶液变为(血)红色,且保持30s不变,
故答案为:溶液变为(血)红色,且保持30s不变;
③NH4SCN标准溶液的平均体积为29.00mL,则NH4SCN的物质的量为0.1000mol•L-1×0.029L=2.9×10-3 mol,根据Ag++SCN-=AgSCN↓可知硝酸银的质量为2.9×10-3 mol×170g/mol×$\frac{100}{25}$=1.972g,所以硝酸银的质量分数为$\frac{1.972g}{2.000g}$×100%=98.60%,
故答案为:98.60%.
点评 本题考查制备实验方案的设计,涉及氧化还原反应、物质的分离提纯、物质含量测定、沉淀滴定原理应用等,综合性较强,基本属于拼合型题目,题目难度中等.


科目:高中化学 来源: 题型:解答题
 非血红素铁是食物中铁存在的形式之一,主要是三价铁与蛋白质和羧酸结合成络合物.
非血红素铁是食物中铁存在的形式之一,主要是三价铁与蛋白质和羧酸结合成络合物.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
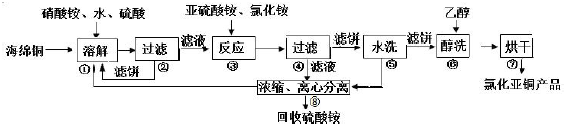
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
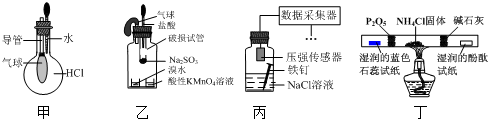
| A. | 用装置甲验证HCl气体易溶于水 | |
| B. | 用装置乙验证SO2具有漂白性 | |
| C. | 用装置丙采集到的压强数据判断铁钉发生析氢腐蚀还是吸氧腐蚀 | |
| D. | 用装置丁检验NH4Cl分解产生的气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
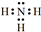 .
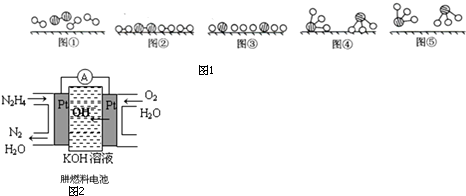
.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 铜中含有大量的有机物,可采用灼烧的方法除去有机物 | |
| B. | 灼烧后含有少量铜的可能原因是该条件下铜无法被氧气氧化 | |
| C. | 通过途径Ⅱ实现用粗制氧化铜制取胆矾,必须进行的实验操作步骤:酸溶、加热通氧气、过滤、蒸发、冷却结晶、过滤、自然干燥 | |
| D. | 与途径II相比,产生等量的胆矾途径I消耗硫酸少,途径I不会产生污染大气的气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com