


 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:
| A、碳酸镁 | B、氢氧化钠 |
| C、氨水 | D、碳酸钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、v(A)=0.15 mol?L-1?min-1 |
| B、v(B)=0.02 mol?L-1?s-1 |
| C、v(C)=0.40 mol?L-1?min-1 |
| D、v(D)=0.45 mol?L-1?min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
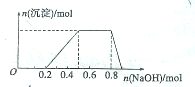
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、热稳定性:NaHCO3>Na2CO3 |
| B、等物质的量浓度的Na2CO3溶液和NaHCO3溶液,前者pH小 |
| C、NaHCO3和Na2CO3的与等物质的量浓度的稀盐酸反应,NaHCO3反应速率更快 |
| D、等物质的量的NaHCO3和Na2CO3的与足量稀盐酸反应,NaHCO3放出的CO2多 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、25℃时,pH=13的1.0L Ba(OH)2溶液中含有的OH-数目为0.2NA |
| B、1.5 mol NO2与足量H2O反应,转移的电子数为2NA |
| C、室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA |
| D、标准状况下,22.4 L己烷中共价键数目为19NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Si可用于制造半导体材料 |
| B、氧化镁、氧化铝可用作耐火材料 |
| C、福尔马林溶液可用作浸泡海产品,进行保鲜 |
| D、过氧化钠可用作呼吸面具中氧气的来源 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com