
铁和铁的化合物用途广泛。请回答下列问题:
(1)写出在潮湿空气中钢铁锈蚀时正极反应的电极反应式:_______________________。
将生锈的铁屑放入H2SO4溶液中充分溶解后,在溶液中并未检测出Fe3+,用离子方程式说明原因:______________________________________。
(2)爱迪生蓄电池的反应式为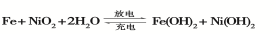
①爱迪生蓄电池的正极是 , 该电池工作一段时间后必须充电,充电时生成Fe的反应类型是______。
②高铁酸钠(Na2FeO4)是一种新型净水剂。用如图装置可以制取少量高铁酸钠。写出在用电解法制取高铁酸钠时,阳极的电极反应式___________________________________。
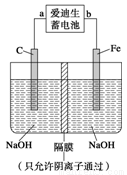
③你认为高铁酸钠作为一种新型净水剂的理由错误的是 ______。
a.高铁酸钠溶于水形成一种胶体,具有较强的吸附性
b.高铁酸钠在消毒杀菌时被还原生成Fe3+,Fe3+水解产生氢氧化铁胶体能吸附悬浮杂质
c.高铁酸钠具有强氧化性,能消毒杀菌
d.高铁酸钠具有强还原性,能消毒杀菌
(3)某FeO、Fe2O3混合物中,铁、氧的物质的量之比为4︰5,其中Fe2+与Fe3+物质的量之比为___________。
(1)O2+2H2O+4e-=4OH- (1分);2Fe3++Fe=3Fe2+(1分) Fe2O3+6H+=2Fe3++3H2O(不写不扣分)
(2)①NiO2(1分);还原反应(1分)
②该反应中的电解质是氢氧化钠,要想生成高铁酸钠,铁电极必需参与电极反应,因此铁电极作的是阳极,涉及到的反应为:Fe-6e-+8OH-=FeO42-+4H2O(2分)
③ad(2分)
(3)1:1(2分)
【解析】
试题分析:(1)在潮湿空气中钢铁锈蚀发生的是吸氧腐蚀,正极反应的电极反应式:O2+2H2O+4e-=4OH- (1分);没有三价铁离子是因为被铁还原了:2Fe3++Fe=3Fe2+(1分) Fe2O3+6H+=2Fe3++3H2O(不写不扣分)
(2)①放电过程中,铁作电池的负极,那么正极一定是NiO2(1分);充电时三价铁生成铁单质,得到电子,一定发生还原反应(1分)
②Fe-6e-+8OH-=FeO42-+4H2O(2分)
③a.高铁酸钠溶于水形成一种胶体,具有较强的吸附性,这种说法是错误的,因为高铁酸钠溶于水时,高铁酸钠作为强氧化剂,对水中的病菌氧化杀毒,被还原为三价铁离子,三价铁离子水解生成氢氧化铁胶体,对水起净化作用,并不是高铁酸钠溶于水成胶体;b.高铁酸钠在消毒杀菌时被还原生成Fe3+,Fe3+水解产生氢氧化铁胶体能吸附悬浮杂质,正确;
c.高铁酸钠具有强氧化性,能消毒杀菌,正确;
d.高铁酸钠具有强还原性,能消毒杀菌,错误,因此选ad(2分)
(3)FeO、Fe2O3混合物中,铁、氧的物质的量之比为4︰5,设其中FeO为xmol、Fe2O3为ymol则有如下关系式:x+2y=4; x+3y=5,解之得:x=2,y=1,所以其中Fe2+与Fe3+物质的量之比为1:1(2分)
考点:考查电化学、铁离子的水解的知识,以及高铁酸钠的性质。


科目:高中化学 来源:2016届云南省高一下学期第一次月考化学试卷(解析版) 题型:选择题
下列化合物中阴离子半径和阳离子半径之比最大的是 ( )
A.LiI B.NaBr C.KCl D.CsF
查看答案和解析>>
科目:高中化学 来源:2015届福建省四地六校高二下学期第一次月考化学试卷(解析版) 题型:选择题
下列各组元素性质的递变情况错误的是( )
A.Li、Be、B原子最外层电子数依次增多
B.C、P、S元素最高正价依次升高
C.N、O、F电负性依次增大
D.Na、K、Rb第一电离能逐渐增大
查看答案和解析>>
科目:高中化学 来源:2015届湖南省益阳市高二下学期第一次月考化学试卷(解析版) 题型:选择题
分子式为C5H11Cl的同分异构体共有(不考虑立体异构)( )
A.6种 B.7种 C.8种 D.9种
查看答案和解析>>
科目:高中化学 来源:2015届湖南省益阳市高二下学期第一次月考化学试卷(解析版) 题型:选择题
脑白金又名褪黑素,据报道它具有提高免疫力、促进睡眠等功效,其结构简式为:
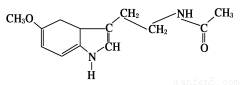
下列关于脑白金说法不正确的是( )
A.能发生加成反应
B.属于芳香族化合物
C.分子式为C13H18N2O2
D.能使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源:2015届湖北省黄石市高二上学期期末考试化学试卷(解析版) 题型:选择题
难挥发性二硫化钽(TaS2 )可采用如下装置提纯。将不纯的TaS2 粉末装入石英管一端,抽真空后引入适量碘并封管,置于加热炉中。反应如下: TaS2(g)+ 2I2(g) TaI4(g) + S2(g),下列说法错误的是
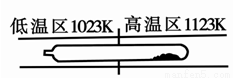
A.在不同温度区域,TaI4 的量不同
B.在提纯过程中,S2 的量不断增多
C.该反应的平衡常数不随TaI4 和S2 的浓度增大而增大
D.在提纯过程中,I2 的作用是将TaS2 从高温区转移到低温区
查看答案和解析>>
科目:高中化学 来源:2015届湖北省黄石市高二上学期期末考试化学试卷(解析版) 题型:选择题
在下列各溶液中,离子一定能大量共存的是
A.强酸性溶液中:K+、Al3+、CH3COO-、SO42-
B.水电离出来的c(H+)=10-13mol/L的溶液:K+、HCO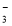 、Br-、Ba2+
、Br-、Ba2+
C.室温下,pH=1的无色溶液中:NH4+、Mg2+、SO42-、Cl-
D.室温下,pH=1的溶液中:Na+、Fe2+、NO3-、SO42-
查看答案和解析>>
科目:高中化学 来源:2015届湖北省高二上学期期末考试化学试卷(解析版) 题型:选择题
x、y、z三种物质的分子组成分别符合烷烃、烯烃、炔烃的通式,若在一定条件下V L
的x、y、z的混合气体可与V L H2发生加成反应,则混合气体中x、y、z的体积比可能是
①1:1:1 ②1:2:3 ③1:4:1 ④3:2:1
A.①③ B.②③ C.③④ D.①④
查看答案和解析>>
科目:高中化学 来源:2015届湖北省荆门市高二上学期期末考试化学试卷(解析版) 题型:填空题
如图为相互串联的甲、乙两电解池。试回答:
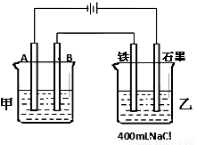
(1)若甲电解池利用电解原理在铁上镀铜,则A是 、 (填电极材料和电极名称),电极反应是 ;B是(要求同A) 、 ,电极反应是 ,应选用的电解质溶液是 ;乙电解池中若滴入少量酚酞试液,开始电解一段时间,铁极附近呈 色。
(2)若甲电解池阴极增重1.28g,乙电解池中剩余溶液仍为400mL,则电解后所得溶液中新生成溶质的物质的量浓度为 mol/L,溶液的pH等于 。
(3)若甲电解池以I=0.21A的电流电解60min后阴极增重0.25g,则此实验测得的阿伏加德罗常数NA为多少(已知电子电量e—=1.60×10—19C)?(简要写计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com