
1 mol 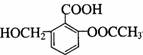 与足量NaOH溶液完全反应,消耗的NaOH的物质的量 为( )
与足量NaOH溶液完全反应,消耗的NaOH的物质的量 为( )
A.1 mol B.2 mol C.3 mol D.4 mol
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
 2NH3(g)△H=-92.2kJ/mol
2NH3(g)△H=-92.2kJ/mol 2NH3(g)△H=-92.2kJ/mol
2NH3(g)△H=-92.2kJ/mol
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
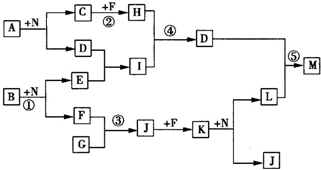 如右框图反应中所涉及的l4种物质都是由短周期元素组成的.已知:
如右框图反应中所涉及的l4种物质都是由短周期元素组成的.已知: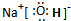
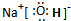
| ||
| △ |
| ||
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
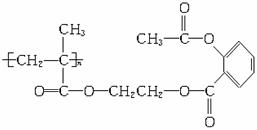
A.n mol B.2n mol C.3n mol D.4n mol
查看答案和解析>>
科目:高中化学 来源: 题型:
某药物结构简式如下图所示,该物质1 mol与足量NaOH溶液反应,消耗NaOH的物质的量为( )
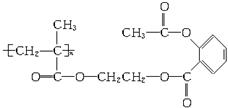
A.n mol B.2n mol C.3n mol D.4n mol
查看答案和解析>>
科目:高中化学 来源: 题型:
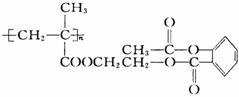
该物质1 mol与足量的NaOH溶液反应,消耗NaOH的物质的量是( )
A.3 mol B.4 mol C.3 n mol D.4 n mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com