
【题目】用纯净的CaCO3与100mL稀盐酸反应制取CO2,实验过程记录如图所示(CO2的体积已折算为标准状况下的体积),下列分析正确的是( )
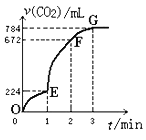
A.F点收集到的CO2的量最多
B.OE段表示的平均速率最快
C.EF段用盐酸表示该反应的平均反应速率为0.4mol·L-1min-1
D.OE、EF、FG三段中,该反应用二氧化碳表示的平均反应速率之比为2:6:7
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是(NA表示阿伏加德罗常数的值)( )
A. 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl- 个数为NA
B. 标准状况下,18 g H2O所占的体积约是22.4 L
C. 32 g O2在标准状况下所占的体积约为22.4 L
D. 2.4g金属镁变为镁离子时失去的电子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究含硒工业废水的处理工艺,对控制水体中硒超标具有重要意义。
(1)已知:H2SeO3为二元弱酸,Ka1(H2SeO3)=3.5×10-3,Ka2(H2SeO3)=5.0×10-8。用离子交换树脂处理含Na2SeO3浓度较高的废水时,发生的交换反应为SeO32-+2RCl=R2SeO3+2Cl- (R为离子交换树脂的树脂骨架)。经离子交换法处理后,废水的pH将________(填“增大”“减小”或“不变”)。
(2)木炭包覆纳米零价铁除硒法是一种改良的含硒废水处理方法。
①以木屑和FeCl3·6H2O为原料,在N2氛围中迅速升温至600 ℃,保持2 h,过程中木屑先转化为木炭,最终制得木炭包覆纳米零价铁。制备木炭包覆纳米零价铁过程中,木炭的作用有吸附和________________________________________。
②木炭包覆纳米零价铁在碱性废水中形成许多微电池,加速SeO32-的还原过程。SeO32-在微电池正极上转化为单质Se,其电极反应式为________。
(3) 绿锈[FeaⅡFebⅡ(OH)cXd](X代表阴离子,Ⅱ、Ⅲ表示铁元素的价态)中铁元素以结构态和游离态两种形式存在。由于结构态的双金属氢氧化物层间存在较大的空隙,形成了巨大的比表面积,同时结构态的FeⅡ还原能力优于游离态的FeⅡ,使得绿锈成为一种良好的除硒剂。
①结构态的绿锈具有优异的吸附性能,而且游离态的Fe3+还易水解生成Fe(OH)3胶体进一步吸附SeO32-。写出Fe3+水解的离子方程式:________。
②不同FeⅡ/FeⅢ组成的绿锈对SeO32-去除效果的影响结果如图1所示。随着绿锈组成中FeⅡ/FeⅢ比值的增大,绿锈的除硒效果先减小后增大的原因可能是________。
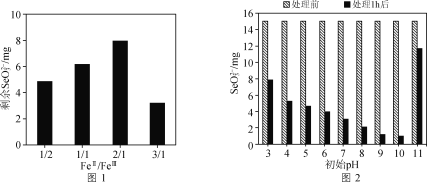
③废水的初始pH会对绿锈去除SeO32-的效果产生影响,关系如图2所示。当初始pH增大至11时,SeO32-的去除效果突然迅速减小的原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LDFCB是锂离子电池的一种电解质,该电解质阴离子由同周期元素W、X、Y、Z构成(如下图),Y的最外层电子数等于X的核外电子总数,四种元素最外层电子数之和为20。下列说法正确的是( )
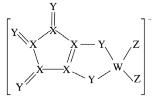
A.四种元素的单质中,Z的沸点最高
B.原子半径∶W>X>Y>Z
C.W、Z形成的分子中各原子均满足8电子稳定结构
D.Y分别与另外三种元素形成的二元化合物中,Y的价态相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为2L的密闭容器中,一定条件下发生化学反应:2NO(g)+2CO(g)![]() N2(g)+2CO2(g) △H= -746.4 kJ·mol-1。起始反应时 NO和CO各为 4 mol,10 秒钟后达到化学平衡,测得N2为1 mol。下列有关反应速率的说法中,正确的是( )
N2(g)+2CO2(g) △H= -746.4 kJ·mol-1。起始反应时 NO和CO各为 4 mol,10 秒钟后达到化学平衡,测得N2为1 mol。下列有关反应速率的说法中,正确的是( )
A. 反应前5秒钟内,用NO表示的平均反应速率为0.lmol·L-1·s-1
B. 达到平衡后,升髙温度,正反应速率将减小,逆反应速率将增大
C. 达到平衡后,反应速率的关系有:V正(CO)=2v逆(N2)
D. 保持容器体积不变,往容器中充入1 mol O2,正、逆反应速率都不改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列热化学反应方程式:
(1)1mol硫酸和氢氧化钠溶液反应放出114.6kJ热量,写出表示中和热的热化学反应方程式____________。
(2)0.5molC2H5OH(l)完全燃烧放出683.4kJ热量,写出表示C2H5OH燃烧热热化学反应方程式________。
(3)24g碳与适量H2O(g)反应吸收262.6kJ热量_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验现象不能充分说明相应的化学反应是放热反应的是
选项 | A | B | C | D |
反应装置或图像 |
|
|
|
|
实验现象或图像信息 | 反应开始后,针筒活塞向右移动 | 反应开始后,甲侧液面低于乙侧液面 | 温度计的水银柱上升 | 反应开始后,气球慢慢胀大 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应:2NO2![]() 2NO+O2在密闭容器反应,达到平衡状态的标志是()
2NO+O2在密闭容器反应,达到平衡状态的标志是()
(1)单位时间内生成n mol O2的同时生成2n mol NO2
(2)单位时间内生成n mol O2的同时生成2n mol NO
(3)用NO2、NO、O2的物质的量浓度变化表示反应速率的比为2:2:1的状态
(4)混合气体的颜色不再改变的状态
(5)混合气体的平均相对分子质量不再改变的状态.
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com