
【题目】下列说法中不正确的是( )
A.ABn型分子中,若中心原子没有孤对电子,则ABn为空间对称结构,属于非极性分子
B.SO3、![]() 、
、![]() 、
、![]() 的空间构型均为三角锥形
的空间构型均为三角锥形
C.NH3、![]() 、H2O、H3O+、CH4中的N、O、C原子均是采取sp3杂化的
、H2O、H3O+、CH4中的N、O、C原子均是采取sp3杂化的
D.配合物[Cu(H2O)4]SO4中,中心离子是Cu2+,配位体是H2O,配位数是4
【答案】B
【解析】
A. ABn型分子中,若中心原子没有孤对电子,则ABn为空间对称结构,正电中心与负电中心重合,属于非极性分子,A正确;
B. SO3、![]() 、
、![]() 、
、![]() 的中心原子孤电子对数分别为0、0、0、1,价层电子对数分别为3、3、3、4,所以SO3、
的中心原子孤电子对数分别为0、0、0、1,价层电子对数分别为3、3、3、4,所以SO3、![]() 、
、![]() 为平面三角形,
为平面三角形,![]() 为三角锥形,B错误;
为三角锥形,B错误;
C. NH3、![]() 、H2O、H3O+、CH4中的N、O、C原子杂化轨道数都是4,均是采取sp3杂化的,只不过NH3、H2O、H3O+中孤对电子占据着杂化轨道,C正确;
、H2O、H3O+、CH4中的N、O、C原子杂化轨道数都是4,均是采取sp3杂化的,只不过NH3、H2O、H3O+中孤对电子占据着杂化轨道,C正确;
D. 配合物[Cu(H2O)4]SO4中,中心离子Cu2+提供空轨道,配位体H2O中氧原子提供孤电子对,形成配位键,配位数是4,D正确。
答案选B。


 学业测评一课一测系列答案
学业测评一课一测系列答案科目:高中化学 来源: 题型:
【题目】某化学课外小组用右图装置制取溴苯并探究该反应的类型。先向分液漏斗中加入苯和液溴,再将混合液滴入反应器A(A下端活塞关闭)中。

(1)写出A中反应的化学方程式:________________________________________。
(2)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是_________________________。
(3)C中盛放CCl4的作用是_____________________________。
(4)若要证明苯和液溴发生的是取代反应,而不是加成反应,通常有两种方法,请按要求填写下表。
向试管D中加入的试剂 | 能证明苯与液溴发生取代反应的现象 | |
方法一 | _____________ | _________________ |
方法二 | _____________ | _________________ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应产生的气体,在标准状况下体积最大的是( )
A.将1molMnO2加入足量浓盐酸中,加热
B.将lmolNa2O2加入足量水中
C.将1molCu加入足量稀硝酸中,加热
D.将1molC加入足量浓硫酸中,加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯化氮(NCl3)是一种淡黄色的油状液体,下面对于NCl3的描述不正确的是( )
A.NCl3为三角锥形B.NCl3是一种极性分子
C.它还能再以配位键与Cl-结合D.NCl3的挥发性比PBr3要大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是
A.碳酸钠的水溶液呈碱性:CO32-+2H2O ![]() H2CO3+2OH-
H2CO3+2OH-
B.用CH3COOH溶解CaCO3:CO32-+CH3COOH=CH3COO-+H2O+CO2↑
C.向Fe (OH)3胶体中加入氢碘酸溶液:Fe(OH)3+3H+=Fe3++3H2O
D.氯化亚铁溶液中通入氯气:2Fe2++Cl2=2Fe3++2Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来,德国研究人员利用O2、N2、CH4、NH3、H2O和HCN这6种远古地球上存在的简单物质,再使用硫醇和铁盐等物质模拟当时环境,成功制得核酸的4种基本模块。下列说法正确的是( )
A.O2的沸点比N2的低
B.NH3分子呈三角锥形
C.配离子[Fe(H2O)6]3+中H与中心原子配位
D.元素C、N、O、S的第一电离能依次增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式错误的是( )
A.AgCl悬浊液中加入KI,沉淀由白色变为黄色:AgCl+I-=AgI+C1-
B.用惰性电极电解MgCl2溶液:2Cl-+2H2O![]() H2↑+Cl2↑+2OH-
H2↑+Cl2↑+2OH-
C.CaCO3与FeCl3溶液反应:3CaCO3+2Fe3++3H2O=3Ca2++2Fe(OH)3↓+3CO2↑
D.向沸水中滴加饱和氯化铁溶液得到红褐色液体:Fe3++3H2O![]() Fe(OH)3(胶体) +3H+
Fe(OH)3(胶体) +3H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】HCN是常见的化工原料,其有机衍生物往往以甙的形式广泛存在于植物界中。
(1)HCN中三种元素的电负性从大到小的顺序为___。
(2)室温时HCN的Ka=6.2×10-10,写出HCN的电离方程式:___;向NaCN溶液中通入CO2,发生反应的离子方程式为___(H2CO3的Ka1=4.45×10-7、Ka2=4.7×10-11)。
(3)已知下列热化学反应:
N2(g)+3H2(g)=2NH3(g) ΔH1=-91.8kJ·mol-1
C(s)+2H2(g)=CH4(g) ΔH2=-75.0kJ·mol-1
H2(g)+2C(s)+N2(g)=2HCN(g) ΔH3=+270.0kJ·mol-1
则反应NH3(g)+CH4(g)=HCN(g)+3H2(g)的ΔH=___kJ·mol-1。
(4)测定木薯肉水解产物中HCN含量的步骤如下:称取ag木薯肉进行水解,将产生的HCN蒸出,用V1mLc1mol·L-1Hg(NO3)2溶液吸收HCN,[Hg(NO3)2+2HCN=Hg(CN)2+2HNO3];以NH4Fe(SO4)2·12H2O作指示剂,用c2mol·L-1KSCN标准溶液滴定上述剩余的Hg(NO3)2,[Hg(NO3)2+2KSCN=Hg(SCN)2+2KNO3];滴定至终点时消耗KSCN溶液V2mL。该木薯肉样品中所含HCN的质量分数c(HCN)=___(用c1、c2、V1、V2表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】贝凡洛尔是一种用于治疗高血压的药物,其中间体F的一种合成路线如下:
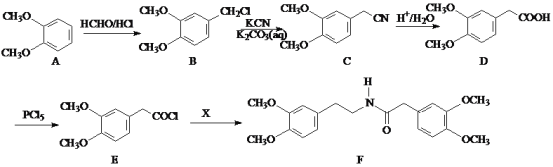
(1)D中含氧官能团名称为______和______。
(2)B→C的反应类型为______。
(3)在Ni催化下C与H2反应可得X,X的分子式为C10H15O2N,写出X的结构简式______。
(4)写出同时满足下列条件的D的一种同分异构体的结构简式______。
①属于芳香化合物,能发生银镜反应和水解反应 ②分子中只有4种不同化学环境的氢
(5)请以![]() 和
和![]() 为原料制备
为原料制备 ,写出该制备的合成路线流程图______。
,写出该制备的合成路线流程图______。
(无机试剂任用,合成路线流程图示例见本题题干)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com