
| A、CH4、C2H6 |
| B、C2H4、C3H6 |
| C、C2H2、C6H6 |
| D、C5H10、C6H6 |
| y |
| 4 |
| 6 |
| 4 |
| 6 |
| 4 |
| 2 |
| 4 |
| 6 |
| 4 |
| 10 |
| 4 |
| 6 |
| 4 |
| y |
| 4 |


科目:高中化学 来源: 题型:
| ||
| 电池 | 电解池 | |
| A | H+移向Pb电极 | H+移向Pb电极 |
| B | 每消耗3molPb | 生成2molAl2O3 |
| C | 正极:PbO2+4H++2e-=Pb2++2H2O | 阳极:2Al+3H2O-6e-=Al2O3+6H+ |
| D |  |  |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加水,将湿润的红色石蕊试纸放在试管口 |
| B、加NaOH溶液,加热,将湿润的红色石蕊试纸放在试管口 |
| C、加NaOH溶液,加热,滴入酚酞试剂 |
| D、加NaOH溶液,加热,滴入紫色石蕊试剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
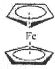 )是一种典型的金属有机化合物,实验室常用新制氯化亚铁和环戊二烯在碱性条件下反应得到.反应原理为FeCl2+2C5H6+2KOH→Fe(C5H5)2+2KCl+2H2O.二茂铁的熔点为172~173℃,在100℃开始升华.能溶于乙醚、二甲亚砜等溶剂,不溶于水,对碱和非氧化性酸稳定.某研究小组设计的实验方案和制备装置示意图如下:
)是一种典型的金属有机化合物,实验室常用新制氯化亚铁和环戊二烯在碱性条件下反应得到.反应原理为FeCl2+2C5H6+2KOH→Fe(C5H5)2+2KCl+2H2O.二茂铁的熔点为172~173℃,在100℃开始升华.能溶于乙醚、二甲亚砜等溶剂,不溶于水,对碱和非氧化性酸稳定.某研究小组设计的实验方案和制备装置示意图如下: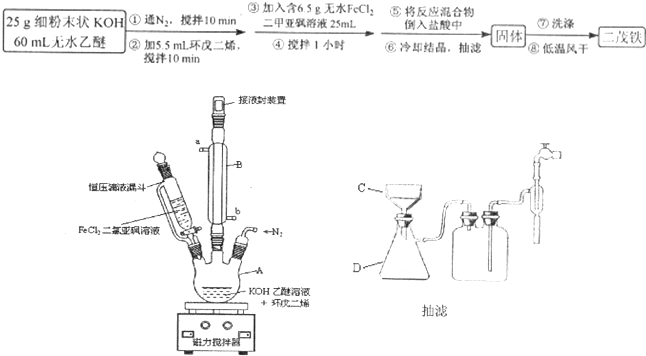
查看答案和解析>>
科目:高中化学 来源: 题型:
| 丁 |
| 丁 |
| 甲 |

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com