
 ;
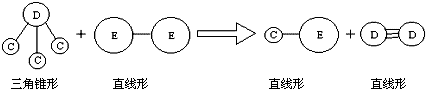
;分析 短周期元素A、B、C、D、E,①常温下,A元素的单质在空气或浓硫酸中,表面都能生成致密的氧化膜,则A为Al元素;②B元素的原子序数比A元素大,B处于第三周期,B原子的次外层的电子数是最外层电子数的2倍,最外层电子数为4,则B为Si元素;③E与A同周期,E的单质为双原子分子,通过单键形成,则E为Cl元素,D与C形成DC3,为三角锥型结构,D的单质通过三键形成的双原子分子,则D为氮元素、C为氢元素,据此解答.
解答 解:短周期元素A、B、C、D、E,①常温下,A元素的单质在空气或浓硫酸中,表面都能生成致密的氧化膜,则A为Al元素;②B元素的原子序数比A元素大,B处于第三周期,B原子的次外层的电子数是最外层电子数的2倍,最外层电子数为4,则B为Si元素;③E与A同周期,E的单质为双原子分子,通过单键形成,则E为Cl元素,D与C形成DC3,为三角锥型结构,D的单质通过三键形成的双原子分子,则D为氮元素、C为氢元素,
(1)A元素最高价氧化物为Al2O3,与NaOH溶液反应的离子方程式为:Al2O3+2OH-═2AlO2-+H2O,
故答案为:Al2O3+2OH-═2AlO2-+H2O;
(2)C为N元素,原子结构示意图为: ,故答案为:
,故答案为: ;
;
处于元素周期表中第二周期第ⅤA族,故答案为:二、ⅤA;
(3)B元素与E元素的最高价氧化物的水化物分别为H2SiO3、HClO4,硅酸为弱酸,高氯酸为强酸,酸性:HClO4>H2SiO3,
故答案为:HClO4>H2SiO3;
(4)氯气在工业上可以用于制备漂白粉等,反应方程式为:2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O,
故答案为:2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O.
点评 本题考查结构性质位置关系用于,难度不大,注意根据分子空间结构与化学键判断元素.


科目:高中化学 来源: 题型:选择题
| A. | 石墨比金刚石稳定 | |
| B. | 金刚石比石墨稳定 | |
| C. | 1mol石墨比1mol金刚石的总能量高 | |
| D. | 1mol石墨和1mol金刚石的总能量相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | FeBr2溶液中通入少量Cl2:Fe2++Cl2═Fe3++2Cl- | |
| B. | 金属钠跟水反应2Na+2H2O═2Na++2OH-+H2↑ | |
| C. | 碳酸钡溶于醋酸BaCO3+2H+═Ba2++H2O+CO2↑ | |
| D. | 向NH4HSO4溶液中逐滴加入Ba(OH)2溶液至刚好沉淀完全Ba2++2OH-+NH4++H++SO42-═BaSO4↓+NH3•H2O+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (A-x+n)mol | B. | (A-x-n)mol | C. | (A-x+n)n/Amol | D. | (A-x-n)n/Amol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 将一定质量的Mg和Al的混合物投入2.0mol/L,250mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入一定浓度的NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如右图所示.回答下列问题:
将一定质量的Mg和Al的混合物投入2.0mol/L,250mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入一定浓度的NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如右图所示.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质(杂质) | 除去杂质 所需试剂或方法 | 离子方程式(若无离子方程式,则写化学方程式) |
| Fe(Al) | ||
| CO2(HCl) | ||
| NaHCO3溶液(Na2CO3) | ||
| Al2O3(Al(OH)3) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
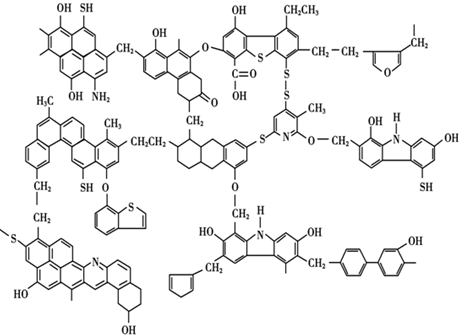
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,请推测其具有的化学性质,填写下列空白:
,请推测其具有的化学性质,填写下列空白:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |
| 原子半径(10-10m) | 1.52 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 0.71 |
| 最高价态 | +1 | +1 | -- | +3 | +4 | +5 | +7 | +1 | +5 | -- |
| 最低价态 | -- | -- | -2 | -- | -4 | -3 | -1 | -- | -3 | -1 |
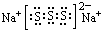 .
.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com