
| A、上述反应中,N2是还原剂,Al2O3是氧化剂 |
| B、上述反应中,每生成1 molAlN需转移3 mol电子 |
| C、AlN中氮元素的化合价为+3 |
| D、AlN的摩尔质量为41g |
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案科目:高中化学 来源: 题型:
| A、c(Ag+)≠c(Cl-),c(Ag+)?c(Cl-)≠Ksp(AgCl) |
| B、c(Ag+)≠c(Cl-),c(Ag+)?c(Cl-)=Ksp(AgCl) |
| C、c(Ag+)=c(Cl-),c(Ag+)?c(Cl-)≠Ksp(AgCl) |
| D、c(Ag+)=c(Cl-),c(Ag+)?c(Cl-)=Ksp(AgCl) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、镀层破损后白铁(镀锌铁)比马口铁(镀锡铁)中的铁更易腐蚀 |
| B、SO2(g)+2H2S(g)═3S(s)+2H2O(l) 在常温下能自发进行,则该反应的△H>0 |
| C、0.1 mol?L-1CH3COOH溶液中加入少量水,CH3COOH电离程度和溶液pH均增大 |
| D、在N2+3H2?2NH3平衡体系中加入少量催化剂,反应速率和平衡常数均增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
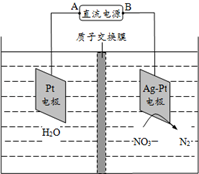 化学市场应用于环境保护.硝酸盐在消化道中可被还原成亚硝酸盐,亚硝酸盐可将低铁红蛋白氧化成高铁红蛋白,使之失去输氧能力,亚硝酸盐还可与仲胺类化合物反应生成亚硝胺类的致癌物质.长期饮用含高浓度硝酸盐的水,会使人畜中毒.目前关于硝酸盐危害的报道主要是“蓝婴儿综合征”.催化反硝化法和电化学降解法可用于治理水中硝酸盐的污染.电化学降解NO3-的原理如图所示:
化学市场应用于环境保护.硝酸盐在消化道中可被还原成亚硝酸盐,亚硝酸盐可将低铁红蛋白氧化成高铁红蛋白,使之失去输氧能力,亚硝酸盐还可与仲胺类化合物反应生成亚硝胺类的致癌物质.长期饮用含高浓度硝酸盐的水,会使人畜中毒.目前关于硝酸盐危害的报道主要是“蓝婴儿综合征”.催化反硝化法和电化学降解法可用于治理水中硝酸盐的污染.电化学降解NO3-的原理如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SO2 |
| B、NO3- |
| C、Fe3+ |
| D、Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、2 H2O2
| ||||
B、2 Al(OH)3
| ||||
C、Fe2O3+3 CO
| ||||
| D、Cl2+2 NaOH═NaCl+NaClO+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、+4 | B、+5 | C、+6 | D、+7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com