
【化学——选修3:物质结构与性质】(15分)
卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们。
(1)卤族元素位于元素周期表的_________区;溴的价电子排布式为____________________。
(2)在一定浓度的溶液中,氢氟酸是以二分子缔合(HF)2形式存在的。使氢氟酸分子缔合的作用力是________。
(3)请根据下表提供的第一电离能数据判断,最有可能生成较稳定的单核阳离子的卤素原子是_________。
氟 | 氯 | 溴 | 碘 | |
第一电离能 (kJ/mol) | 1681 | 1251 | 1140 | 1008 |
(4)已知碘酸(HIO3)和高碘酸(H5IO6)的结构分别如图I、II所示:

请比较二者酸性强弱:HIO3_____ H5IO6(填“>”、“<”或“=”)。
(5)已知ClO2-为角型,中心氯原子周围有四对价层电子。ClO2-中心氯原子的杂化轨道类型为___________,写出一个ClO2-的等电子体__________。
(6)下图为碘晶体晶胞结构。有关说法中正确的是_____________。
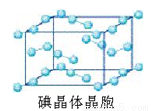
A.碘分子的排列有2种不同的取向,2种取向不同的碘分子以4配位数交替配位形成层结构
B.用均摊法可知平均每个晶胞中有4个碘原子
C.碘晶体为无限延伸的空间结构,是原子晶体
D.碘晶体中存在的相互作用有非极性键和范德华力
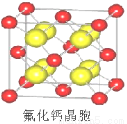
(7)已知CaF2晶体(见下图)的密度为ρg/cm3,NA为阿伏加德罗常数,棱上相邻的两个Ca2+的核间距为a cm,则CaF2的相对分子质量可以表示为___________。
科目:高中化学 来源:2014-2015学年江西省上饶市高三第二次高考模拟化学试卷(解析版) 题型:选择题
SO2通入BaCl2溶液中并不产生沉淀,而通入另一种气体后可以产生白色沉淀。则图中右侧Y形管中放置的药品组合不符合要求的是(必要时可以加热)

A.Cu和浓硝酸 B.大理石和稀盐酸
C.CaO和浓氨水 D.高锰酸钾溶液和浓盐酸
查看答案和解析>>
科目:高中化学 来源:2014-2015黑龙江省哈尔滨市高一下学期第一次月考化学试卷(解析版) 题型:选择题
氨水呈弱碱性的原因是
A.通常状况下,氨气的溶解度较大
B.氨水中的NH3·H2O电离出少量的OH-
C.溶于水的氨气生成的少量NH3·H2O全部电离生成OH-
D.氨气本身的碱性弱
查看答案和解析>>
科目:高中化学 来源:2014-2015黑龙江省哈尔滨市高二下学期第一次月考化学试卷(解析版) 题型:选择题
下列物质中,不能使酸性高锰酸钾溶液褪色的是
A.乙烯 B.乙炔 C.苯 D.甲苯
查看答案和解析>>
科目:高中化学 来源:2014-2015甘肃省张掖市高三第三次诊断考试理综化学试卷(解析版) 题型:选择题
在2 L的密闭容器中进行如下反应:CO(g)+H2O(g)
 CO2(g)+H2(g),有如下数据:
CO2(g)+H2(g),有如下数据:
实验 | 温度/℃ | 起始量/mol | 平衡量/mol | |||
CO | H2O | CO2 | H2 | CO2 | ||
1 | 650 | 2.0 | 1.0 | 0 | 0 | 0.8 |
2 | 800 | 2.0 | 2.0 | 0 | 0 | 1.0 |
下列说法正确的是
A.正反应为放热反应
B.实验1中,CO的转化率为80%
C.650℃时,化学平衡常数K=
D.实验1再加入1.0 mol H2O,重新达到平衡时,n(CO2)为1.6 mol
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省宁波市高三十校联考理科综合化学试卷(解析版) 题型:实验题
(共14分)乳酸亚铁([CH3CH(OH)COO]2Fe·3H2O,Mr=288)是一种常用的补铁剂,可通过乳酸与碳酸亚铁反应制得:CH3CH(OH)COOH+FeCO3+2H2O→[CH3CH(OH)COO]2Fe·3H2O+CO2↑。
已知FeCO3易被氧化:4FeCO3+6H2O+O2=4Fe(OH)3+4CO2
某兴趣小组用FeCl2(用铁粉和稀盐酸制得)和NH4HCO3制备FeCO3的装置示意图如下:
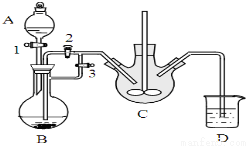
回答下列问题:
(1)NH4HCO3盛放在装置 中(填字母),该装置中涉及的主要反应的离子方程式 _
(2)将生成的FeCl2溶液和NH4HCO3溶液混合时的操作是 _
(3)将制得的FeCO3加入到足量乳酸溶液中,再加入少量铁粉,75℃下搅拌反应。铁粉的作用是 。反应结束后,无需过滤,除去过量铁粉的方法是 _
(4)该兴趣小组用KMnO4法测定样品中亚铁含量进而计算产品中乳酸亚铁的质量分数,发现产品的质量分数总是大于100%,其原因可能是 。
经查阅文献后,该兴趣小组改用铈(Ce)量法测定产品中Fe2+的含量。取2.880g产品配成100mL溶液,每次取20.00mL,进行必要处理,用0.1000mol·L-1Ce(SO4)2标准溶液滴定至终点,平均消耗Ce(SO4)2 19.70mL。滴定反应如下:
Ce4++Fe2+=Ce3++Fe3+
则产品中乳酸亚铁的质量分数为 _
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省协作体高三下学期联考理科综合化学试卷(解析版) 题型:选择题
在一个恒容绝热的密闭容器中,发生可逆反应:M(?) + 2N(g) P(g) + Q(g) △H>0 ,已知M的状态未知,则下列描述一定达到平衡的标志是
P(g) + Q(g) △H>0 ,已知M的状态未知,则下列描述一定达到平衡的标志是
①当物质M、N、P的体积分数比为 1 : 1 : 1时
②混合气体的密度不变时
③体系的温度不变时
④反应速率2v (N)正=v (Q)逆时
⑤体系的压强不变时
⑥气体的平均相对分子质量不变时
A.①③④ B.③⑥ C.②③⑥ D.③④⑤
查看答案和解析>>
科目:高中化学 来源:2014-2015山西省原平市高二上学期期末考试化学试卷(解析版) 题型:选择题
下列有机物实际存在且命名正确的是
A.2,2-二甲基丁烷 B.2-甲基-5-乙基-1-己烷
C.3-甲基-2-丁烯 D.3,3-二甲基-2-戊烯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com