
【题目】亚硝酸钠被称为工业盐,不能用作食品工业,但在漂白、电镀等方面应用广泛.现以木炭、浓硝酸、水和铜为原料生成的一氧化氮与过氧化钠反应制备亚硝酸钠的装置如图所示(部分夹持装置略).
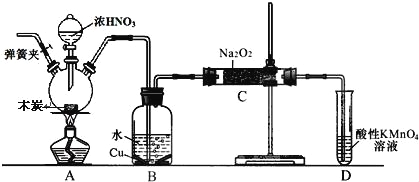
已知:室温下,①2NO+Na2O2=2NaNO2②3NaNO2+3HCl═3NaCl+HNO3+2NO↑+H2O;③酸性条件下,NO或NO2﹣ 都能与MnO4﹣反应生成NO3﹣ 和Mn2+
完成下列填空:
(1)写出浓硝酸与木炭反应的化学方程式 .
(2)B中观察到的主要现象是有无色气体产生和 ,D装置的作用是 .
(3)检验C中产物有亚硝酸钠的方法是 .
(4)经检验C产物中除亚硝酸钠外还含有副产物碳酸钠和氢氧化钠,为避免产生这些副产物应在B、C装置间增加装置,则该装置中盛放的药品名称 .
(5)将7.8g过氧化钠完全转化成为亚硝酸钠,理论上至少需要木炭 g.
【答案】(1)C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O;
CO2↑+4NO2↑+2H2O;
(2)铜片逐渐溶解,溶液变为蓝色; 吸收未反应的NO;
(3)取样,加入稀盐酸,产生无色气体,遇到空气变为红棕色;
(4)碱石灰;
(5)1.8.
【解析】
试题分析:(1)加热条件下,C和浓硝酸反应生成二氧化碳、二氧化氮和水;
(2)生成的二氧化氮进入B中和水反应生成硝酸,硝酸和铜反应生成硝酸铜、NO和水;
生成硝酸的同时还生成NO,NO有毒不能直接排空;
(3)亚硝酸钠和稀盐酸反应生成生成NO,NO不稳定易被空气氧化生成红棕色气体;
(4)碱石灰能吸收水和二氧化碳,但不能吸收NO;
(5)n(Na2O2)=![]() =0.1mol,根据2NO+Na2O2=2NaNO2、3NO2+H2O=2HNO3+NO、C+4HNO3(浓)
=0.1mol,根据2NO+Na2O2=2NaNO2、3NO2+H2O=2HNO3+NO、C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O计算需要C的质量.
CO2↑+4NO2↑+2H2O计算需要C的质量.
解:(1)加热条件下,C和浓硝酸反应生成二氧化碳、二氧化氮和水,反应方程式为C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O,故答案为:C+4HNO3(浓)
CO2↑+4NO2↑+2H2O,故答案为:C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O;
CO2↑+4NO2↑+2H2O;
(2)生成的二氧化氮进入B中和水反应生成硝酸,硝酸和铜反应生成硝酸铜、NO和水,所以看到的现象是:有无色气体生成且Cu逐渐溶解、溶液变蓝色;
生成硝酸的同时还生成NO,NO有毒不能直接排空,过氧化钠和NO反应生成亚硝酸钠,所以过氧化钠的作用是吸收未反应的NO,
故答案为:铜片逐渐溶解,溶液变为蓝色; 吸收未反应的NO;
(3)亚硝酸钠和稀盐酸反应生成NO,NO不稳定,易被空气中氧气氧化生成红棕色二氧化氮,所以其检验方法是取样,加入稀盐酸,产生无色气体,遇到空气变为红棕色,故答案为:取样,加入稀盐酸,产生无色气体,遇到空气变为红棕色;
(4)碱石灰能吸收水和二氧化碳,但不能吸收NO,为防止副反应发生,增加装置中盛放的药品是碱石灰,故答案为:碱石灰;
(5)n(Na2O2)=![]() =0.1mol,根据2NO+Na2O2=2NaNO2知,0.1mol过氧化钠反应需要0.2molNO,根据3NO2+H2O=2HNO3+NO知生成0.2molNO需要0.6mol二氧化氮、根据C+4HNO3(浓)
=0.1mol,根据2NO+Na2O2=2NaNO2知,0.1mol过氧化钠反应需要0.2molNO,根据3NO2+H2O=2HNO3+NO知生成0.2molNO需要0.6mol二氧化氮、根据C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O知生成0.6mol二氧化氮需要0.15molC,则C的质量=12g/mol×0.15mol=1.8g,
CO2↑+4NO2↑+2H2O知生成0.6mol二氧化氮需要0.15molC,则C的质量=12g/mol×0.15mol=1.8g,
故答案为:1.8.


科目:高中化学 来源: 题型:
【题目】【化学——选修2:化学与技术】
某工厂用软锰矿(含MnO2约70% 及A12O3)和闪锌矿(含ZnS约80%及FeS)共同生产MnO2和Zn(干电池原料)。
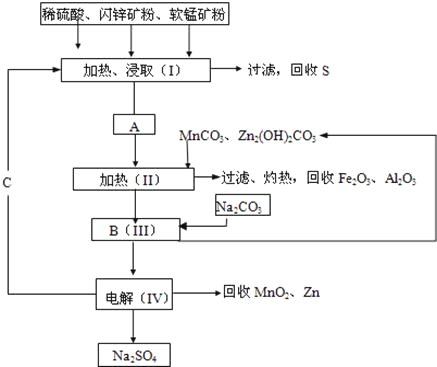
已知:①A是![]() 的混合液。
的混合液。
②IV中的电解方程式为:![]()
(l)A中属于还原产物的是________________________。
(2)加人MnCO3、Zn2(OH)2CO3的作用 ________________________。
II需要加热的原因是:____________________。C的化学式是 _______________。
(3)该生产中除得到MnO2和Zn以外,还可得到的副产品是_________________。
(4)如果不考虑生产中的损耗,除矿石外,需购买的化工原料是_____________。
(5)要从Na2SO4溶液中得到芒硝(Na2SO4·10H2O),需进行的操作有蒸发浓缩、___________、过滤、洗涤、干燥等。
(6)从生产MnO2和Zn的角度计算,软锰矿和闪锌矿的质量比大约是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,0.2mol·L-1的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是

A.HA为强酸
B.该混合液pH=7
C.图中X表示HA,Y表示OH-,Z表示H+
D.该混合溶液中:c(A-)+c(Y)=c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组对生石灰与水反应是显著放热反应进行了实验探究,在除了用手触摸式竹壁感觉发热外,还设计了下列几个可行性方案。
甲方案:将温度计与盛放有生石灰的小试管用橡皮筋捆绑在一起,放入有水的小烧杯中,用胶头滴管向小试管中缓缓滴入水,看到的现象是______,说明反应放热。(下列装置中支撑及捆绑等仪器己略去)
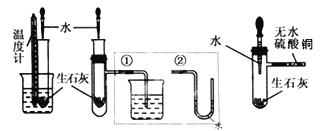
乙方案:将盛放有生石灰的小试管插入带支管的试管中,支管接①或②,用胶头滴管向小试管中缓缓滴入水,看到的现象是(接①)________(接②)________,说明反应放热。
丙方案:用胶头滴管向盛放有生石灰且带支管的试管中滴加水,支管接的导管中盛适量无水硫酸铜粉末,看到的现象是______________,说明反应放热,其原因是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:下表为25℃时某些弱酸的电离平衡常数。
CH3COOH | HClO | H2CO3 |
Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.4×10-7 Ka2=4.7×10-11 |
下图表示常温下,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化。下列说法正确的是

下列说法正确的是
A.相同浓度的CH3COONa和NaClO的混合溶液中,各离子浓度的大小关系是:c(Na+)> c(ClO-)> c(CH3COO-)> c(OH-)> c(H+)
B.向NaClO溶液中通入少量二氧化碳的离子方程式为:ClO-+CO2+ H2O =HClO+CO32-
C.图像中a、c两点处的溶液中![]() 相等(HR代表CH3COOH或HClO)
相等(HR代表CH3COOH或HClO)
D.图像中a点酸的总浓度大于b点酸的总浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分某实验室需要配制480mL0.10mol/LNa2CO3溶液。
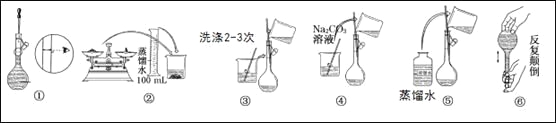
(1)实验时,应用托盘天平称取十水和碳酸钠晶体________g。
(2)所需玻璃仪器有:玻璃棒、烧杯、100mL量筒、__________、________。
(3)实验时图中所示操作的先后顺序为________ (填编号)。
(4)在配制过程中,下列操作对所配溶液浓度有无影响?__________(填“偏高”、“偏低”或“无影响”)
①称量时误用“左码右物”
②转移溶液后没有洗涤烧杯和玻璃棒
③向容量瓶加水定容时俯视液面
④摇匀后液面下降,再加水至刻度线
(5)若改用浓溶液稀释,需要量取2mol/LNa2CO3溶液____________mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列与实验相关的叙述正确的是
A. 稀释浓硫酸时,应将蒸馏水沿玻璃棒缓慢注入浓硫酸中
B. 配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出
C. 盛放NaOH溶液时,使用带玻璃瓶塞的磨口瓶
D. 检验某溶液是否含有SO42-时,应取少量该溶液,依次加入稀盐酸和BaCl2溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【改编题】当你走进化学实验室时,首先要认真阅读并遵守《实验室安全守则》。以下实验室中的学生行为不符合实验室安全规范的是(回答两条即可):

(1)_____________________________________________________
(2)_____________________________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com