
在体积不变的400 ℃恒温密闭容器中,一定量的SO2与1 mol O2在催化剂作用下发生反应:
2SO2(g)+O2(g)  2SO3(g) ΔH =-Q kJ ∕ mol(Q﹥0)。当气体的物质的量减少0.5 mol
2SO3(g) ΔH =-Q kJ ∕ mol(Q﹥0)。当气体的物质的量减少0.5 mol
时反应达到平衡。下列叙述错误的是
A.增大氧气浓度,平衡正向移动,平衡常数不变
B.降低温度,正反应速率比逆反应速率减小的程度小
C.平衡时SO2气体的转化率为50%
D.该条件下反应放出0.5Q kJ的热量
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源:2016届河北省衡水市高三上一轮复习检测一化学试卷(解析版) 题型:选择题
下列叙述不正确的是( )
① 熔点:金刚石>晶体硅>单质硫
② 气态氢化物的稳定性:H2O>HF>H2S
③ 同一主族元素的氢化物,相对分子质量越大,它的沸点一定越高
④ 因为常温下白磷可自燃,而氮气需要在放电时才与氧气反应,所以非金属性:P>N
⑤ 碱性氧化物一定是金属氧化物
A.①②③ B.②③④ C.②④⑤ D.①③⑤
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高二上期末化学试卷(解析版) 题型:选择题
下列事实中,不能用勒夏特列原理加以解释的是
A.醋酸溶液加水稀释醋酸的电离程度增大
B.工业合成氨时常用通过过量的氮气的方法提高氢气的转化率
C.新制的氯水在光照的条件下颜色变浅
D.氯化铁溶液中加Fe粉振荡后颜色变浅
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高二上期末化学卷(解析版) 题型:选择题
用惰性电极电解一定量的硫酸铜溶液,实验装置如下图甲。电解过程中的实验数据如下图乙,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中产生气体的总体 积(标准状况)。则下列说法不正确的是

A.电解过程中,a电极表面先有红色物质析出,后有气泡产生
B.b电极上发生反应的方程式为:4OH--4e-=2H2O+O2↑
C.曲线O~P段表示O2的体积变化
D.从开始到Q点时收集到的混合气体的平均摩尔质量为12 g/mol
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高二上期末化学卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中能大量共存的是 ( )
A.pH=1的溶液中:Fe2+、NO3-、Na+、SO42-
B.水电离出的c(H+) =10-12mol/L的溶液中:Ca2+、K+、Cl-、HCO3-
C.c(H+)/c(OH-)=1012的水溶液中:NH4+、Al3+、NO3-、Cl-
D.c(Fe3+) =0.1mol/L的溶液中:K+、ClO-、SO42-、SCN-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省滕州市高一上学期12月月考化学试卷(解析版) 题型:填空题
Ⅰ、碳元素是日常生活中接触非常多的一种元素,回答下列问题。
(1)用化学方程式表示溶洞生成的反应原理: 。
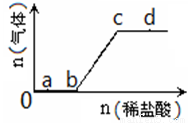
(2)可用稀盐酸来鉴别Na2CO3和NaHCO3溶液,现将稀盐酸慢慢滴入碳酸钠溶液中,请写出开始阶段发生反应的离子方程式 。
(3)写出用小苏打来治疗胃酸过多时发生反应的离子方程式: 。
II、氮元素在生命活动中扮演着重要的角色,回答下列与氮及其化合物有关的问题:
(1)德国化学家哈伯、波施等科学家成功地开发了将氮气转化为氨气的生产工艺。请用化学方程式表示工业合成氨的反应原理: 。
写出在氨气的出气口处,检验有氨气生成的操作:
(2)将氨气通入酚酞溶液中,酚酞溶液变成红色。请用方程式解释原因: 。
Ⅲ、印刷电路板是由塑料和铜箔复合而成,刻制印刷电路时要用FeCl3溶液作为“腐蚀液”溶解铜。
(1)写出该反应的离子方程式: ;
(2)从使用过的腐蚀液中可以回收金属铜,下列试剂能实现的是 (填序号)
A.氯气 B.铁 C.硝酸 D.稀硫酸
(3)向使用过的腐蚀液中通入Cl2,可使Fe2+转化为Fe3+,写出反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省邵阳市高一上学期第三次月考化学试卷(解析版) 题型:选择题
在无色强酸性溶液中,下列各组离子能够大量共存的是
A.Cl -、Na+、NO3-、Ca2+ B.NH4+、HCO3-、Cl-、K+
C.K+、Ba2+、Cl-、SO42- D.Cu2+、NH4+、I-、Cl-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省济宁市高一上12月阶段测化学试卷(解析版) 题型:推断题
在下列各变化中,E为无色无味的液体(常温下),F为淡黄色粉末,G为常见的无色气体(反应条件均已省略)。回答下列问题:

(1) 写出反应②的化学反应方程式 ,在该反应中,每生成2.24LG(标准状况),该反应转移电子的物质的量是 。
(2)若反应①在溶液中进行,A、C、D均含氯元素,且A中氯元素的化合价介于C和D之间。则反应①的化学方程式是 。
(3)若反应①在溶液中进行,A是一种强酸,B是一种含两种金属元素的盐,当A过量时,C及D均易溶于水。则A过量时反应①的离子反应方程式是 。
查看答案和解析>>
科目:高中化学 来源:2016届吉林省高三上学期第五次模拟理综化学试卷(解析版) 题型:选择题
化工生产中常用FeS作沉淀剂除去工业废水中的Cu2+:Cu2+(aq)+FeS(s) CuS(s)+Fe2+(aq)下列有关叙述中正确的是( )
CuS(s)+Fe2+(aq)下列有关叙述中正确的是( )
①FeS的Ksp大于CuS的Ksp
②该反应平衡常数K=
③溶液中加入少量Na2S固体后,溶液中c(Cu2+)、c(Fe2+)保持不变
④达到平衡时c(Fe2+)=c(Cu2+)
A.②③ B.①③④ C.①② D.②③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com