
(1)镀铜可防止铁制品腐蚀,若用铜盐进行化学镀铜,应选用__________(填“氧化剂”或“还原剂”)与之反应。电镀时镀件与电源的极连接。
(2)利用如图装置,可以模拟铁的电化学防护。
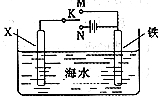
若X为碳棒,为减缓铁的腐蚀,开关K应该置于__________处。若X为锌,开关K置于M处,该电化学防护法称为__________。
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源:2017届黑龙江省高三10月月考化学卷(解析版) 题型:填空题
工业上电解制碱的技术是用离子交换膜法,主要原料是饱和食盐水.
请回答下列问题:
(1)阳离子交换膜把电解槽隔成了阴极室和阳极室,电解食盐水时,它只允许 (填离子符号)通过。
(2)为了去除粗盐中混有的Ca2+、Mg2+、SO42-.下列选项中所加试剂(均为溶液)及加入顺序均合理的是 (填选项字母)
A.先加足量的BaCl2,再加足量的Na2CO3,最后加入适量稀盐酸
B.先加入足量的NaOH.再加入足量的BaCl2,然后加入足量Na2CO3,最后加入适量稀盐酸
C.先加足量的Na2CO3,再加足量的BaCl2,然后加足量的NaOH,最后加入适量稀盐酸.
D.先加足量的Ba(NO3)2,再加足量NaOH,然后再加足量的Na2CO3,最后加入适量稀盐酸.
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上.在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过.

图中X、Y分别是 、 (填化学式),分析比较图示中氢氧化钠质量分数 a、b、c的从大到小的顺序为
分别写出燃料电池中正极、负极上发生的电极反应正极: ;负极: ;
这样设计的主要节(电)能之处在于(任写出一条)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省四地六校高一上第一次月考化学试卷(解析版) 题型:选择题
漂白粉的主要成分是( )
A.NaClO B.CaCl2和 Ca(ClO)2 C.NaCl和NaClO D.Ca(ClO)2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省四地六校高二上第一次月考化学试卷(解析版) 题型:选择题
已知1 mol H2(g)完全燃烧生成H 2O(g)放出热量a kJ,且氧气中1 mol O===O键完全断裂时吸收能量b kJ,H 2O中1 mol H—O键形成时放出能量c kJ,H 2中1 mol H—H键断裂时吸收的能量为( )
A.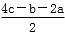 kJ B.
kJ B.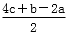 kJ C.(4c+b-2a) kJ D.(4c-b+2a) kJ
kJ C.(4c+b-2a) kJ D.(4c-b+2a) kJ
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省四地六校高二上第一次月考化学试卷(解析版) 题型:选择题
已知化学反应A2(g)+B2(g)== 2AB(g)的能量变化如图所示,则下列叙述中正确的是:( )
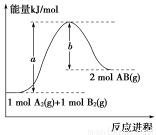
A.该反应的反应热ΔH=+(a-b)kJ/mol
B.每生成2分子AB吸收b kJ热量
C.该反应中反应物的总能量高于生成物的总能量
D.断裂1 mol A—A和1 mol B—B键,放出a kJ能量
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省高二上第一次月考化学卷(解析版) 题型:选择题
在密闭容器中充入4molSO2和3molO2,一定条件下建立平衡:2SO2(g)+O2(g) 2SO3(g)ΔH=-QkJ/mol,测得SO2的转化率为90%,则反应放出的热量为( )
2SO3(g)ΔH=-QkJ/mol,测得SO2的转化率为90%,则反应放出的热量为( )
A.2QkJ B.1.8QkJ C.QkJ D.0.9QkJ
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省高二上第一次月考化学卷(解析版) 题型:选择题
关于铅蓄电池的说法正确的是( )
A.在放电时,正极发生的反应是Pb(s)+SO42—(aq)-2e—=PbSO4(s)
B.在充电时,电池中硫酸的浓度不断变大
C.在放电时,该电池的正极材料是铅板
D.在充电时,阳极发生的反应是PbSO4(s)+2e—=Pb(s)+SO42—(aq)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省高一上10月月考化学试卷(解析版) 题型:选择题
m g某二价金属M溶于足量盐酸中,标况下放出氢气n L,则金属M的相对原子质量为 ( )
A.n/m B.2m/n C. n /(22.4 m) D.22.4m/n
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高二第二次月考化学试卷(解析版) 题型:选择题
为增强铝的耐腐蚀性,现以铅蓄电池为外电源,以Al作阳极、Pb作阴极,电解稀硫酸,使铝表面的氧化膜增厚。其反应原理如下:
电池:Pb(s)+PbO2(s)+2H2SO4(aq)=2PbSO4(s)+2H2O(l);
电解池:2Al+3H2O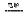 Al2O3+3H2↑
Al2O3+3H2↑
电解过程中,以下判断正确的是( )
电池 | 电解池 | |
A | H+移向Pb电极 | H+移向Pb电极 |
B | 每消耗3molPb | 生成1molAl2O3 |
C | 正极:PbO2+4H++2e—=Pb2++2H2O | 阳极:2Al+3H2O-6e—=Al2O3+6H+ |
D |
|
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com