
| A. | 0.1 mol/L | B. | 0.2 mol/L | C. | 0.4 mol/L | D. | 0.6mol/L |
分析 反应生成硫酸铝、硫酸铁,硫酸可能有剩余,向反应后的混合溶液中加入100mLNaOH溶液,恰好使Al3+、Fe3+完全沉淀,此时溶液中溶质为Na2SO4,根据钠离子守恒有n(NaOH)=2n(Na2SO4),根据硫酸根守恒有n(Na2SO4)=n(H2SO4),据此计算n(NaOH),再根据c=$\frac{n}{V}$计算.
解答 解:反应生成硫酸铝、硫酸铁,硫酸可能有剩余,向反应后的混合溶液中加入10mLNaOH溶液,恰好使Al3+、Fe3+完全沉淀,此时溶液中溶质为Na2SO4,根据硫酸根守恒有n(Na2SO4)=n(H2SO4)=0.2L×0.05mol/L=0.01mol,根据钠离子守恒有n(NaOH)=2n(Na2SO4)=0.02mol,则该NaOH溶液的物质的量浓度=$\frac{0.02mol}{0.1L}$=0.2mol/L,故选B.
点评 本题考查混合物计算、物质的量浓度有关计算,难度中等,注意利用守恒法解答,侧重对学生思维能力、分析处理问题能力的考查.


科目:高中化学 来源: 题型:选择题
| A. | 给试管里的固体加热时,试管口应略向下倾斜,外壁干燥后再预热 | |
| B. | 给试管里的液体加热时.试管口应略向上倾斜(约45°),外壁干燥后再预热 | |
| C. | 加热后的蒸发皿,要用坩埚钳夹持 | |
| D. | 盛装浓硫酸的铁桶,用水冲洗,并用打火机照明 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
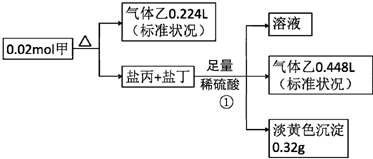
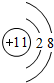 ,甲的化学式Na2S2O4
,甲的化学式Na2S2O4查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 |
| 将打磨过的铝片(过量)放入一定浓度的氯化铜溶液中 | 产生气泡,析出疏松的红色固体,溶液逐渐变为无色 |
| 反应结束后分离出溶液备用 | |
| 红色固体用蒸馏水洗涤后,置于潮湿的空气中 | 一段时间后固体由红色变为绿色[视其主要成分为Cu2(OH)2CO3] |
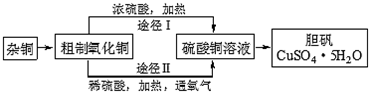
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应证明O2能氧化PtF6 | |
| B. | 22.4LO2参加反应时,转移1mol电子 | |
| C. | O2PtF6中既有离子键又有共价键 | |
| D. | 68.2g O2PtF6中含有1.204×1024个分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 操作 | 现象 | 结论或目的 |
| (1)取少量溶液于试管中,向溶液中加入足量NaCl溶液 | - | 除尽Ag+ |
| (2)取少量上述溶液于试管中,加入KSCN溶液,振荡 | 溶液变血红色 | 存在Fe3+ |
| (3)取(1)中少量上述溶液于试管中,加入酸性KMnO4溶液,振荡 | 血红色消失 | 存在Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 49 | B. | 50 | C. | 51 | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A~F是初中化学常见的六种物质,它们之间的关系如图所示.“→”表示物质间的转化关系,“--”表示两种物质能相互反应(部分反应物、生成物及反应条件未标出).A可以与酸、碱、盐三类物质发生反应,D是食盐的主要成分,C和F都是无色气体,反应①和②都有白色沉淀生成.
A~F是初中化学常见的六种物质,它们之间的关系如图所示.“→”表示物质间的转化关系,“--”表示两种物质能相互反应(部分反应物、生成物及反应条件未标出).A可以与酸、碱、盐三类物质发生反应,D是食盐的主要成分,C和F都是无色气体,反应①和②都有白色沉淀生成.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com