
【题目】下列化学用语描述错误的是( )
A.H2O的电子式![]()
B.Cl﹣的结构示意图 ![]()
C.NH4Cl为离子化合物
D.质量数为37的氯原子3717Cl
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在一定条件下,将3 mol A 和 1 mol B 两种气体混合于固定容积为 2 L 的密闭容器中,发生如下反应: 3A(g)+B(g) ![]() xC(g)+2D(g)。 2 min 末该反应达到平衡,测得生成 0.8 mol D,0.4 molC。下列判断正确的是( )
xC(g)+2D(g)。 2 min 末该反应达到平衡,测得生成 0.8 mol D,0.4 molC。下列判断正确的是( )
A. x=2 B. 2 min 时, A 的浓度为 1.2mol·L-1
C. 2 min 内 A 的反应速率为 0.6 mol·L-1·min-1 D. B 的转化率为 60%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的原电池装置,X、Y为两电极,电解质溶液为稀硫酸,外电路中的电子流向如图所示,对此装置的下列说法正确的是
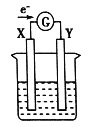
A. 外电路的电流方向为:X→外电路→Y
B. 若两电极分别为Zn和石墨棒,则X为石墨棒,Y为Zn
C. 若两电极都是金属,则它们的活泼性为X>Y
D. X极上发生的是还原反应,Y极上发生的是氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学兴趣小组的同学在完成课本乙醇制乙醛的实验后,改进了实验方案(如图)按下列顺序进行如下实验操作.
①连接好仪器,检验装置的气密性;
②正确添加试剂;
③点燃C装置中的酒精灯;
④向圆底烧瓶中滴加10%过氧化氢溶液;
⑤点燃B装置中的酒精灯加热无水乙醇至沸腾并持续加热.
根据以上所有内容回答下列问题:
(1)装置e的作用是;
(2)写出d中发生反应的化学方程式;
(3)为检验D中收集的产物中是否含有乙醛,甲同学利用银氨溶液检验,请写出'化学反应方程式;
(4)该兴趣小组的同学还对乙醛进行银镜反应的最佳实验条件进行了探究(部分实验数据如表):
实验变量 | 银氨溶液的S/mL | 乙醛的量/滴 | 温度/℃ | 反应混合液的pH值 | 出现银镜的时间/min |
1 | 1 | 3 | 65 | 11 | 5 |
2 | 1 | 3 | 45 | 11 | 6.5 |
3 | 1 | 5 | 65 | 11 | 4 |
①实验1和实验2,探究的实验目的是 .
②当银氨溶液的量为1mL,乙醛的量为3滴,温度为55℃,反应混合液pH为11时,出现银镜的时间为 min.(填范围)
(5)若试管中收集到的液体用紫色石蕊试液检验,溶液显红色,说明液体中还含有
(填物质名称),要除去该物质,可先在混合液中加入(填写下列选项中的字母),然
后再通过(填操作名称)即可除去.
A.饱和NaCl溶液 B.C2H5OH C.NaHCO3溶液 D.CCl4 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把0.6 mol X气体和0.6 mol Y气体混合于2L的密闭容器中,使它们发生如下反应3X(g)+Y(g) ![]() nZ(g)+2W(g)。5 min末生成0.2 mol W。若测知以Z的浓度变化表示平均反应速率为0.01 mol·L-1·min-1,则化学方程式中的值为
nZ(g)+2W(g)。5 min末生成0.2 mol W。若测知以Z的浓度变化表示平均反应速率为0.01 mol·L-1·min-1,则化学方程式中的值为
A. 1 B. 2 C. 3 D. 4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(15分)水中溶解氧是水生生物生存不可缺少的条件.某课外小组采用碘量法测定学校周边河水中的溶解氧.实验步骤及测定原理如下:
Ⅰ.取样、氧的固定
用溶解氧瓶采集水样.记录大气压及水体温度.将水样与Mn(OH)2碱性悬浊液(含有KI)混合,反应生成MnO(OH)2 , 实现氧的固定.
Ⅱ.酸化,滴定
将固氧后的水样酸化,MnO(OH)2被I﹣还原为Mn2+ , 在暗处静置5min,然后用标准Na2S2O3溶液滴定生成的I2(2S2O32﹣+I2=2I﹣+S4O62﹣).
回答下列问题:
(1)取水样时应尽量避免扰动水体表面,这样操作的主要目的是 .
(2)“氧的固定”中发生反应的化学方程式为 .
(3)Na2S2O3溶液不稳定,使用前需标定.配制该溶液时需要的玻璃仪器有烧杯、玻璃棒、试剂瓶和;蒸馏水必须经过煮沸、冷却后才能使用,其目的是杀菌、除及二氧化碳.
(4)取100.00mL水样经固氧、酸化后,用a molL﹣1Na2S2O3溶液滴定,以淀粉溶液作指示剂,终点现象为;若消耗Na2S2O3溶液的体积为b mL,则水样中溶解氧的含量为mgL﹣1 .
(5)上述滴定完成后,若滴定管尖嘴处留有气泡会导致测量结果偏 . (填“高”或“低”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在蛋白质溶液中分别进行下列操作或加入下列物质,其中一种与其它三种现象有本质不同的是( )
A.加热
B.加浓硝酸
C.加硫酸铵的浓溶液
D.加硫酸铜溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列4组物质,能起反应的写出化学方程式;属于离子反应的,还要写出离子方程式;不能起反应的,说明不能起反应的原因。
(1)硫酸溶液与氯化钡溶液:_______________________________________;
(2)稀硫酸与碳酸钠溶液:_______________________________________;
(3)硝酸钠溶液与氯化钾溶液:_______________________________________;
(4)碳酸钙和盐酸:_______________________________________________________;
(5)氢氧化钾溶液和醋酸(CH3COOH)溶液:___________________________________;
(6)三氯化铁溶液和氢氧化钾溶液:__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铁具有独有的脱色能力,适用于染料、染料中间体、印染、造纸行业的污水处理.某课题小组设计如下方案制备氯化亚铁并探究氯化亚铁(Fe2+)的还原性.某同学选择下列装置用氯化铁制备少量氯化亚铁(装置不可以重复使用).查阅资料知,氯化铁遇水剧烈水解,在加热条件下氢气还原氯化铁生成FeCl2 . 
(1)实验开始前应先检查装置的气密性,请叙述装置A气密性检验的方法:
(2)气流从左至右,装置接口连接顺序是a
(3)装置C中干燥管中所盛试剂的名称是: , 作用是:
(4)装置D中发生的化学方程式是:
(5)为了测定氯化亚铁的质量分数,某同学进行了如下实验: 称取实验制备的氯化亚铁样品5.435g,配成溶液,用1.00molL﹣1酸性KMnO4标准溶液滴定至终点.(已知还原性Fe2+>Cl﹣)滴定结果如表所示:
滴定次数 | 标准溶液的体积 | |
滴定前刻度/mL | 滴定后刻度/mL | |
1 | 1.04 | 25.03 |
2 | 1.98 | 25.99 |
3 | 3.20 | 25.24 |
①写出滴定过程中所发生的2个离子方程式 ,
②样品中氯化亚铁的质量分数为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com