
下列各离子①R- ②R+ ③R2+ ④R3+ ⑤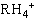 ⑥RH-(R表示不同的元素)都有10个电子,其中不会破坏水的电离平衡的有:( )
⑥RH-(R表示不同的元素)都有10个电子,其中不会破坏水的电离平衡的有:( )
A.仅有①③ B.仅有② C.②③⑥ D.②③⑤
科目:高中化学 来源: 题型:
在水溶液中能大量共存的一组离子是( )
A.Na+、Ba2+、Cl-、NO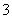
B.Pb2+、Hg2+、S2-、SO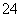
C.NH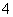 、H+、S2O
、H+、S2O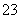 、PO
、PO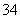
D.Ca2+、Al3+、Br-、CO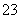
查看答案和解析>>
科目:高中化学 来源: 题型:
已知298 K时,合成氨反应N2(g)+3H2(g)===2NH3(g) ΔH=-92.0 kJ·mol-1,将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应。测得反应放出的热量为(假定测量过程中没有能量损失)( )
A.一定小于92.0 Kj B.一定大于92.0 kJ
C.一定等于92.0 kJ D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验事实不能证明醋酸是弱电解质的是( )
A.相同pH的醋酸溶液和盐酸分别与同样颗粒大小的锌反应时,产生H2的起始速率相等
B.常温下,测得0.1 mol·L-1醋酸溶液的pH=4
C.常温下,将pH=1的醋酸溶液稀释1 000倍,测得pH<4
D.在相同条件下,醋酸溶液的导电性比盐酸的弱
查看答案和解析>>
科目:高中化学 来源: 题型:
一种常用的泡沫灭火器构造如图。内筒a是玻璃瓶,外筒b是钢瓶,平时泡沫灭火器内筒外筒盛有液态试剂,当遇火警时,将灭火器取下倒置,内外筒液体试剂立即混合产生大量CO2泡沫灭火,从液态试剂在灭火器中长久放置和快速灭火两个角度分析,盛放药品正确的是( )
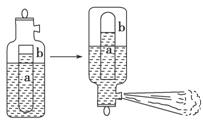 A.a中盛饱和Na2CO3溶液,b中盛Al2(SO4)3溶液
A.a中盛饱和Na2CO3溶液,b中盛Al2(SO4)3溶液
B.a中盛饱和NaHCO3溶液,b中盛Al2(SO4)3溶液
C.a中盛Al2(SO4)3溶液,b中盛饱和Na2CO3溶液
D.a中盛Al2(SO4)3溶液,b中盛饱和NaHCO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
判断以下几种叙述中不正确的是( )
A.某温度下,不论何种水溶液中c(H+)·c(OH-)乘积相等,即水的离子积是一个常数
B.醋酸钠和醋酸的混合液中若c(Na+)=c(CH3COO-),则溶液中c(H+)=c(OH-)
C.如果定义pOH=-lgc(OH-),则常温下某水溶液中的pOH和pH之和等于14
D.某水溶液由于条件的改变,如果氢离子浓度变小,则氢氧根离子浓度一定变大
查看答案和解析>>
科目:高中化学 来源: 题型:
某二元酸(化学式用H2B表示)在水中的电离方程式是:H2B=H++HB-,HB-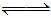 H++B2-。
H++B2-。
回答下列问题:
(1)Na2B溶液显 (填“酸性”、“中性”或“碱性”),理由是
(用离子方程式表示)。
(2)在0.1 mol·L-1 Na2B溶液中,下列粒子浓度关系式正确的是 。
A.c(B2-)+c(HB-)+c(H2B)=0.1 mol·L-1 B.c(Na+)+c(OH-)=c(H+)+c(HB-)
C.c(Na+)+c(H+)=c(OH-)+c(HB-)+2c(B2-) D.c(Na+)=2c(B2-)+2c(HB-)
(3)已知0.1 mol·L-1 NaHB溶液的pH=2,则0.1 mol·L-1H2B溶液中氢离子的物质的量浓度可能是 0.11 mol·L-1(填“<”、“>”或“=”),理由是
。
(4)0.1 mol·L-1 NaHB溶液中各种离子浓度由大到小的顺序是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值。下列叙述正确的是( )
A.98 g H2SO4和H3PO4中含有的氧原子数均为4NA
B.1 L 1 mol·L-1的硫酸与高氯酸(HClO4)溶液中含有的氧原子数均为4NA
C.33.6 L NO2溶解于足量的水中得到硝酸溶液,溶液中NO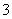 数目为NA
数目为NA
D.32 g铜发生氧化还原反应,一定失去NA个电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com