
分析 (1)具有自由移动的离子或电子可导电;在水溶液中或熔化状态下可导电的化合物为电解质,在水溶液中和熔化状态下均不导电的化合物为非电解质;
(2)①I中加入过量D的溶液,反应生成氯化钠、水、二氧化碳;
②C的溶液中通入少量H,反应生成碳酸钠和水.
解答 解:(1)具有自由移动的离子或电子可导电,能导电的有F I J;在水溶液中或熔化状态下可导电的化合物为电解质,在水溶液中和熔化状态下均不导电的化合物为非电解质,则属于电解质的有A C D G,非电解质的是B E H,
故答案为:F I J;A C D G;B E H;
(2)①I中加入过量D的溶液的离子反应为CO32-+2H+=H2O+CO2↑,故答案为:CO32-+2H+=H2O+CO2↑;
②C的溶液中通入少量H的离子反应为2OH-+CO2=H2O+CO32-,故答案为:2OH-+CO2=H2O+CO32-.
点评 本题考查离子反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,注意复分解反应及电解质的判断,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 升高温度能加快反应速率的主要原因,是增加了反应物分子中活化分子的百分数 | |
| B. | 正反应是吸热反应,达到平衡时,升高温度,v正增大,v逆减小,所以平衡向正反应方向移动 | |
| C. | 一定条件下增大反应物的量,一定会加快反应速率 | |
| D. | 对于任何一个化学反应,用其中任何一种反应物浓度的减小来表示化学反应速率,都是相同的数值 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
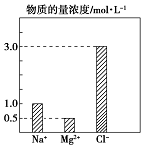 某100mL溶液中含有的部分离子浓度大小如图所示,该溶液可能还含有Fe3+、Ba2+、H+、SO42-、CO32-.为了进一步确认,对该溶液进行实验检测:
某100mL溶液中含有的部分离子浓度大小如图所示,该溶液可能还含有Fe3+、Ba2+、H+、SO42-、CO32-.为了进一步确认,对该溶液进行实验检测:| 实验操作与现象 | 实验结论 | 判断理由 | |
| 步骤一 | 仔细观察坐标图 | 肯定无 CO32- | 肯定无该离子的理由碳酸根离子和镁离子之间会反应 |
| 步骤二 | 该溶液呈无色、透明、均一状态 | 肯定无 Fe3+ | 肯定无该离子的理由该离子为黄色 |
| 步骤三 | 加入足量BaCl2溶液,生成23.3g白色沉淀,再加稀硝酸,沉淀不消失 | 肯定有SO42-、H+;肯定无Ba2+ | 肯定有H+的理由电荷守恒 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在托盘天平的两个托盘上各放一张大小一样的纸,然后将NaOH固体放在纸上进行称量 | |
| B. | 把称量的NaOH固体放入盛有适量蒸馏水的烧杯中,溶解后立即把溶液转移到容量瓶中 | |
| C. | 用蒸馏水洗涤烧杯、玻璃棒2~3次,每次洗涤后的溶液都注入容量瓶中 | |
| D. | 沿着玻璃棒往容量瓶中加入蒸馏水,直到溶液凹液面恰好与刻度相切 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
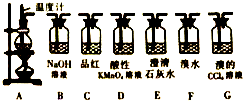 某课外小组利用下列装置,对浓硫酸与乙醇反应的可能产物进行了如下探究.
某课外小组利用下列装置,对浓硫酸与乙醇反应的可能产物进行了如下探究.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
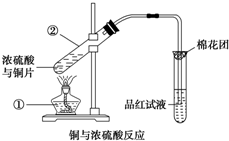 如图是铜与浓硫酸反应的实验装置图,请回答下列问题.
如图是铜与浓硫酸反应的实验装置图,请回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | X | Y |  |
| A | 温度 | 容器内混合气体的密度 | |
| B | A的物质的量 | B的转化率 | |
| C | 催化剂的质量 | C的体积分数 | |
| D | 加入Ar的物质的量 | 逆反应速率 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com