考点:物质的分离、提纯和除杂,离子方程式的书写
专题:离子反应专题
分析:(1)NaHCO3能与氢氧化钠反应生成碳酸钠和水;
(2)NaHCO3不稳定,加热易分解;
(3)氧化铝为两性氧化物,可与强碱反应,则用强碱性溶液可除去氧化铝杂质;
(4)除去FeCl3中混有的FeCl2,可加入氧化剂,但不能引入新的杂质所以选用氯气;
(5)FeCl3可与铁反应生成FeCl2.
解答:
解:(1)NaHCO
3能与氢氧化钠反应生成碳酸钠和水,离子方程式:HCO
3-+OH
-=H
2O+CO
32-,故答案为:HCO
3-+OH
-=H
2O+CO
32-;
(2)NaHCO
3不稳定,加热易分解,可用加热的方法除杂,反应的方程式为:2NaHCO
3Na
2CO
3+H
2O+CO
2↑,故答案为:2NaHCO
3Na
2CO
3+H
2O+CO
2↑;
(3)氧化铝为两性氧化物,可与强碱反应,反应的离子方程式为Al
2O
3+2OH
-=2AlO
2-+H
2O,故答案为:Al
2O
3+2OH
-═2AlO
2-+H
2O;
(4)除去FeCl
3中混有的FeCl
2,可加入氧化剂,但不能引入新的杂质所以选用氯气;反应的离子方程式为Cl
2+2Fe
2+=2Fe
3++2Cl
-,故答案为:2Fe
2++Cl
2=2Fe
3++2Cl
-;
(5)Fe与氯化铁反应生成氯化亚铁,且Fe不能溶于水,选Fe来除杂,发生的离子反应为Fe+2Fe
3+═3Fe
2+,故答案为:2Fe
3++Fe=3Fe
2+.
点评:本题考查除杂及离子反应方程式的书写,为高考常见题型,注意除杂的原则及物质的性质即可解答,侧重氧化还原反应的考查,题目难度不大.



 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案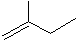 表示的分子式是
表示的分子式是