

| ŹµŃé²Ł×÷ | ĻÖ Ļó | ÓŠ¹ŲµÄ»Æѧ·½³ĢŹ½ |
| ŹµŃéŅ»£ŗȔɣĮæ¹ĢĢåѳʷ£¬ | ³ĪĒåŹÆ»ŅĖ®±ä»ė×Ē | Na2CO3+2HCl=2NaCl+H2O+CO2”ü CO2+Ca(OH)2=CaCO3”ż+H2O |
| ŹµŃ鶞£ŗȔɣĮæ¹ĢĢåѳʷ£¬ ¼ÓĖ®Åä³ÉČÜŅŗ£¬µĪ¼ÓŹŹĮæµÄ ČÜŅŗ | ÓŠ°×É«³Įµķ²śÉś | |
| ŹµŃé²Ł×÷ | ĻÖ Ļó | ÓŠ¹ŲµÄ»Æѧ·½³ĢŹ½ |
| µĪ¼ÓĻ”ŃĪĖį£¬Č»ŗ󽫲śÉśµÄĘųĢåĶØČė³ĪĒåŹÆ»ŅĖ® | ÓŠĘųÅŻ²śÉś | |
| ĀČ»ÆøĘ»ņ ĀČ»Æ±µµČ | | Na2CO3+CaCl2=CaCO3”ż+2NaCl»ņ Na2CO3+BaCl2=BaCO3”ż+2NaClµČ |


 Ó®ŌŚæĪĢĆĆūŹ¦æĪŹ±¼Ę»®ĻµĮŠ“š°ø
Ó®ŌŚæĪĢĆĆūŹ¦æĪŹ±¼Ę»®ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
 X + CO2 + H2O£» ¢Ś Z + CO2
X + CO2 + H2O£» ¢Ś Z + CO2 X + O2 £»
X + O2 £» Y + O2 £» ¢Ü X + Ca(OH)2
Y + O2 £» ¢Ü X + Ca(OH)2 Y + CaCO3
Y + CaCO3 ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®5.28g | B£®4.22g | C£®3.18g | D£®2.12g |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®¶žÕßŌŚĖ®ÖŠµÄČܽā¶Č²»Ķ¬£¬Ģ¼ĖįĒāÄʵÄČܽā¶Č“óÓŚĢ¼ĖįÄʵÄČܽā¶Č |
| B£®¶žÕßČČĪČ¶ØŠŌ²»Ķ¬£¬Ģ¼ĖįÄʵÄČČĪČ¶ØŠŌ“óÓŚĢ¼ĖįĒāÄʵÄČČĪČ¶ØŠŌ |
| C£®¶žÕ߶¼ÄÜÓėŃĪĖį·“Ó¦·Å³ö¶žŃõ»ÆĢ¼ĘųĢ壬µ«²śĘųĮæŗĶ·“Ó¦æģĀż²»Ķ¬ |
| D£®¶žÕßŌŚŅ»¶ØµÄĢõ¼žĻĀ²»ÄÜĻą»„×Ŗ»Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®¼ÓČėµÄNaOHÖŹĮæŅ»¶Ø×īŠ” |
| B£®¼ÓČėµÄNa2O2ŗĶNa2OµÄĪļÖŹµÄĮæÖ®±ČĪŖ1:1 |
| C£®ÖĘ³É±„ŗĶČÜŅŗŗó£¬4·ŻČÜŅŗÖŠĖłŗ¬NaOHÖŹĮæĻąĶ¬ |
| D£®¼ÓČėµÄNaOH”¢Na2O2”¢Na2O”¢NaµÄĪļÖŹµÄĮæÖ®±ČĪŖ2”Ć1”Ć1”Ć2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
| ĪĀ¶Č(”ę) | 10 | 20 | 30 | ¼ÓČČÖó·ŠŗóĄäČ“µ½50”ę |
| pH | 8.3 | 8.4 | 8.5 | 8.8 |
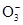 µÄĖ®½ā³Ģ¶ČŌö“󣬹Ź¼īŠŌŌöĒ攣
µÄĖ®½ā³Ģ¶ČŌö“󣬹Ź¼īŠŌŌöĒ攣²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Na2CO3 | B£®Na2CO3ŗĶNaOH | C£®NaHCO3 | D£®NaHCO3ŗĶNa2CO3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com