
洗涤含SO2的烟气。以下物质可作洗涤剂的是________。
a.Ca(OH)2 b.Na2CO3
c.CaCl2 d.NaHSO3
科目:高中化学 来源: 题型:
比较下列四组反应,回答下列问题。
一组:①Na2O2+CO2
②Na2O2+SO2
二组:③Na2O2+FeCl3(溶液)
④Na2O2+FeCl2(溶液)
三组:⑤SO2通入品红溶液中,加热
⑥Na2O2加入到品红溶液中,加热
四组:⑦NaOH溶液滴入紫色石蕊溶液中
⑧Na2O2固体加入到紫色石蕊溶液中
问题:(1)写出①、②两反应的化学方程式。
(2)判断③、④反应中可能发生的现象,为什么?
(3)判断⑤、⑥反应中可能发生的现象,为什么?
(4)判断⑦、⑧反应中可能发生的现象?
查看答案和解析>>
科目:高中化学 来源: 题型:
200 ℃时,11.6 g CO2和H2O的混合物气体与足量的Na2O2反应,反应后固体增加了3.6 g,则原混合物的平均相对分子质量为( )
A.5.8 B.11.6 C.23.2 D.46.4
查看答案和解析>>
科目:高中化学 来源: 题型:
硫酸厂有一辆存放过浓硫酸的铁槽车。某工人违反操作规程,边吸烟边用水冲洗铁槽车,结果发生了爆炸。下列对引起爆炸的原因说法正确的是( )
A.浓硫酸遇明火爆炸
B.浓硫酸遇水发热爆炸
C.铁与水(常温下)反应产生的氧化物爆炸
D.稀释后的硫酸与铁反应产生的氢气在空气中遇明火而爆炸
查看答案和解析>>
科目:高中化学 来源: 题型:
某兴趣小组在实验室用铜和硫酸为原料,采用多种方法制取硫酸铜,制备方法如下:
方法一
(1)浓硫酸试剂瓶上适合贴上的标签是________(填序号)。

(2)甲同学取6.4 g铜片和10 mL 18 mol·L-1浓硫酸,放在试管中共热时发现,铜与热的浓硫酸反应后并没有得到预期的蓝色溶液,而是在试管底部看到灰白色沉淀。甲同学为了验证其中灰白色沉淀的主要成分,设计下列实验:
实验步骤:倾倒掉上层液体后,向所得灰白色的固体中加入适量蒸馏水,边加边搅拌。
实验现象:_________________________________。
实验结论:所得灰白色固体的化学式为__________。
(3)乙还观察到加热过程中,试管内壁上部析出少量淡黄色固体物质,持续加热,淡黄色固体物质又慢慢地溶于浓硫酸而消失。淡黄色固体消失的原因是(用化学方程式回答)________________________________________________________________________。
直到最后反应完毕,发现试管中还有铜片剩余,乙根据自己所学的化学知识,认为试管中还有硫酸剩余。他这样认为的理由是________________________________________________________________________。
方法二
(4)丙同学认为甲设计的实验方案不好,他自己设计的思路是2Cu+O2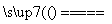 2CuO,CuO+H2SO4===CuSO4+H2O。
2CuO,CuO+H2SO4===CuSO4+H2O。
对比甲的方案,你认为丙同学的优点是①________________________________________________________________________;
②________________________________________________________________________。
方法三
(5)丁同学取一铜片和稀硫酸放在试管中,再向其中滴入双氧水发现溶液逐渐呈蓝色,写出反应的化学方程式________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
锌与100 mL 18.5 mol·L-1的浓硫酸充分反应后,锌完全溶解,同时生成气体甲33.6 L(标准状况)。将反应后的溶液稀释至1 L,测得溶液的pH=1。下列叙述不正确的是( )
A.反应中共消耗1.8 mol H2SO4
B.气体甲中SO2与H2的体积比为4∶1
C.反应中共消耗97.5 g Zn
D.反应中共转移3 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对电子排布图的相关表述正确的是( )
A. 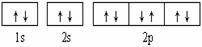 可表示单核10电子粒子基态时电子排布
可表示单核10电子粒子基态时电子排布
B. 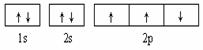 此图错误,违背了泡利原理
此图错误,违背了泡利原理
C. 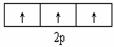 表示基态N原子的价电子排布
表示基态N原子的价电子排布
D.  表示处于激发态的B的电子排布图
表示处于激发态的B的电子排布图
查看答案和解析>>
科目:高中化学 来源: 题型:
前四周期原子序数依次增大的元素A、B、C、D中,A和B的价电子层中未成对电子均只有1个,并且A-和B+的电子数相差为8;与B位于同一周期的C和D,它们价电子层中的未成对电子数分别为4和2,且原子序数相差为2。
(3)A、B和D三种元素组成的一个化合物的晶胞如图所示。
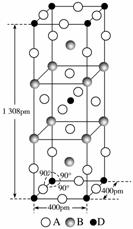
①该化合物的化学式为________;D的配位数为__________;
②列式计算该晶体的密度__________g·cm-3。
(4)A-、B+和C3+三种离子组成的化合物B3CA6,其中化学键的类型有______________;该化合物中存在一个复杂离子,该离子的化学式为__________,配位体是____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com