
| A����ع���ʱ��CO32-�������ƶ� |
| B����طŵ�ʱ��������ӦΪH2+CO32--2e-=CO2��+H2O |
| C�������ĵ缫��ӦΪ��O2+2H2O+4e-=4OH- |
| D��ͨ�����ĵ缫����������Ӧ |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Ca2+��Na+��NO3-��SO42- |
| B��HCO3-��Na+��Cl-��H+ |
| C��Mg2+��Cl-��Cu2+��SO42- |
| D��K+��Ba2+��Cl-��NO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
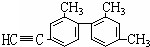 ��֪̼̼���������Ƽ���������ת���ṹ��ʽΪ��ͼ��ʾ����������˵������ȷ���ǣ�������
��֪̼̼���������Ƽ���������ת���ṹ��ʽΪ��ͼ��ʾ����������˵������ȷ���ǣ�������| A�������д���ͬһֱ���ϵ�̼ԭ�������7�� |
| B��������������12��̼ԭ�Ӵ���ͬһƽ���� |
| C�����������ϵ�һ�ȴ��ﹲ��3�� |
| D������������һ�ȴ��ﹲ��5�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����A����B���롰B��A����������A��B��ԭ������ĺ�����ͬ |
| B��ʧ����Խ��Ļ�ԭ�����仹ԭ�Ծ�Խǿ |
| C��������ֻ�ܵõ��ӱ���ԭ���������� |
| D���������Ԫ�صĻ�����һ������ǿ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��250mL 0.4mol/L��ϡ������Һ |
| B��25mL 0.8mol/L��ϡ������Һ |
| C��100mL 1mol/L��ϡ������Һ |
| D��100mL 2mol/L��������Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ȫ�ܽ�89g��������Ҫ1.0mol/L��ϡ��������2L |
| B��������Ļ�ѧʽ��FeO��OH�� |
| C������������Ԫ��Ϊ+3�� |
| D��44.5g������Լ����6.02��1023��Oԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʵ�� | ��Ӧ�¶�/�� | Na2S2O3��Һ | ϡH2SO4 | H2O | ||
| V/mL | c/��mol?L-1�� | V/mL | c/��mol?L-1�� | V/mL | ||
| A | 10 | 15 | 0.2 | 10 | 0.2 | 15 |
| B | 10 | 15 | 0.4 | 5 | 0.4 | 20 |
| C | 35 | 15 | 0.2 | 10 | 0.2 | 15 |
| D | 35 | 15 | 0.4 | 5 | 0.4 | 20 |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���÷�Ӧ���Ȼ�ѧ����ʽΪ��N2H4��l��+2H2O2��l��=N2��g��+4H2O��g����H=-641.6 kJ?mol-1 |
| B���÷�Ӧ��������ԭ�� |
| C���ö���Դ��ͻ���ŵ�֮һ�Ƿ�Ӧ����Ի�������Ⱦ |
| D��Һ̬�µ�ȼ����Ϊ-20.05 kJ?mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������Ħ������ |
| B�������Ħ������ |
| C���������������� |
| D���ܶȡ�Ħ����� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com