
| A. | 简单离子的半径:Y>X | |
| B. | 氢化物的稳定性:Z>W | |
| C. | X与Z形成的化合物溶于水所得溶液显碱性 | |
| D. | Y与W形成的化合物溶于水所得溶液显酸性 |
分析 短周期主族元素X、Y、Z、W的原子序数依次增大,Y元素原子的最外层电子数等于X元素原子的最外层电子数的一半,X处于偶数族,X、Z的原子序数之差为8,二者只能同主族,令Y的最外层电子数为x,则X、Z原子最外层电子数为2x,三种元素原子的最外层电子数之和为15,则x+2x+2x=15,解得x=3,则X为O元素,Y为Al元素,Z为S元素,W为Cl元素,据此解答.
解答 解:短周期主族元素X、Y、Z、W的原子序数依次增大,Y元素原子的最外层电子数等于X元素原子的最外层电子数的一半,X处于偶数族,X、Z的原子序数之差为8,二者只能同主族,令Y的最外层电子数为x,则X、Z原子最外层电子数为2x,三种元素原子的最外层电子数之和为15,则x+2x+2x=15,解得x=3,则X为O元素,Y为Al元素,Z为S元素,W为Cl元素.
A.电子层结构相同的离子,核电荷数越大离子半径越小,故离子半径:O2->Al3+,故A错误;
B.非金属性Z(S)<W(Cl),故氢化物稳定性Z<W,故B错误;
C.X与Z形成的化合物为二氧化硫、三氧化硫,溶于水形成亚硫酸、硫酸,它们的溶于呈酸性,故C错误;
D.Y与W形成的化合物为氯化铝,溶于中铝离子水解,溶液呈酸性,故D正确.
故选:D.
点评 本题考查结构性质位置关系综合应用,侧重对元素周期律的考查,关键是计算确定元素种类,较好的考查学生分析推理能力以及元素化合物知识.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
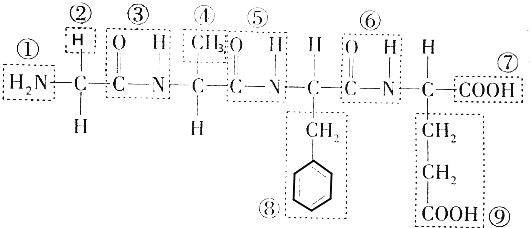
| A. | 能发生脂化反应的酸一定是羧酸 | |
| B. | 蛋白质溶液中加入浓Na2SO4溶液,蛋白质从溶液中凝聚而析出叫盐析 | |
| C. | 天然蛋白质一定条件下水解的最终产物是α-氨基酸 | |
| D. | 淀粉、纤维素和油脂在一定条件下都能发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
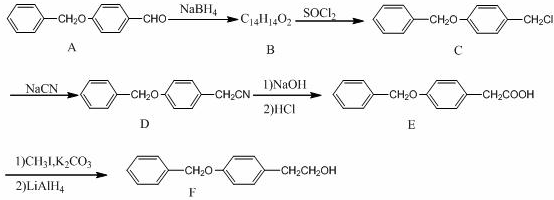
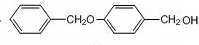 ;由B→C的反应类型是:取代反应.
;由B→C的反应类型是:取代反应. .
. .
.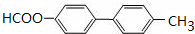 .
. ,请写出以
,请写出以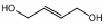 为原料制备化合物X
为原料制备化合物X 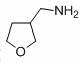 (结构简式见图)的合成路线流程图(无机试剂可任选):
(结构简式见图)的合成路线流程图(无机试剂可任选): .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X、Y、Z在周期表中不可能处于同一周期 | |
| B. | 原子序数Y>X>Z | |
| C. | 简单离子半径:r(X2-)>r(Y+) | |
| D. | Y 单质在X单质中点燃生成物离子个数之比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| Y | ||||
| Q | W | X | Z |
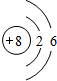 ;举一例说明Z的非金属性比X的非金属性强的事实:酸性强弱;HClO4>H3PO4,或稳定性:HCl>PH3.
;举一例说明Z的非金属性比X的非金属性强的事实:酸性强弱;HClO4>H3PO4,或稳定性:HCl>PH3. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
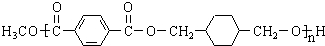 ,某研究小组用芳香烃A为原料合成PCT的合成路线如下.
,某研究小组用芳香烃A为原料合成PCT的合成路线如下.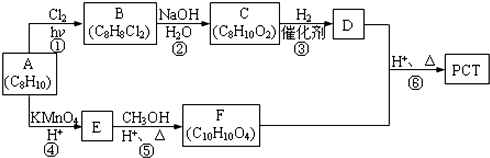
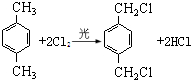 ,A分子中最多有14个原子共平面.
,A分子中最多有14个原子共平面.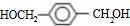 ,反应③的类型是加成反应,
,反应③的类型是加成反应,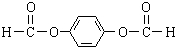 (写结构简式).
(写结构简式).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com