
| A. | 2H2O+O2+4e-=4OH- | B. | Fe-2e-=Fe2+ | ||
| C. | 2H++2e-=H2↑ | D. | Fe-3e-=Fe3+ |
科目:高中化学 来源: 题型:选择题
| A. | 纯锌与稀硫酸反应时,加少量CuSO4溶液,可使反应速率加快 | |
| B. | 甲烷和氧气以及KOH溶液构成的新型燃料电池中,负极上发生的反应为CH4+8OH-+8e-═CO2+6H2O | |
| C. | 把铜片和铁片紧靠在一起浸入稀H2SO4中,铁片表面出现气泡 | |
| D. | 把铜片插入FeCl3溶液中,在铜片表面出现一层铁 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ②③ | C. | ①③ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
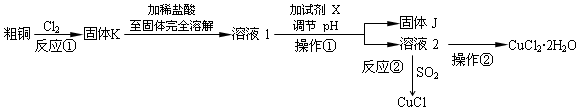
| 平行次数 | 1 | 2 | 3 |
| 0.250g样品消耗硫酸铈标准溶液的体积(mL) | 24.35 | 24.05 | 23.95 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 取20ml 0.1mol/L氨水溶液(其电离常数为K),用0.10mo/L盐酸滴定.滴定过程中溶液PH变化如图所示.图中a、b、c、d四个点所代表的溶液中,c(OH-)≈K的点是( )
取20ml 0.1mol/L氨水溶液(其电离常数为K),用0.10mo/L盐酸滴定.滴定过程中溶液PH变化如图所示.图中a、b、c、d四个点所代表的溶液中,c(OH-)≈K的点是( )| A. | a点 | B. | b点 | C. | c点 | D. | d点 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
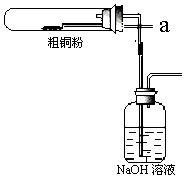
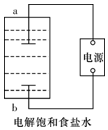 某兴趣小组模拟氯碱工业生产原理并探究其产品的性质.已知文献记载:
某兴趣小组模拟氯碱工业生产原理并探究其产品的性质.已知文献记载:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Q1=Q3=197 kJ | B. | Q1=Q3<197 kJ | C. | 2Q2=Q1<197 kJ | D. | 2Q2<Q1<197 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠和冷水反应:Na+2H2O═Na++2OH-+H2↑ | |
| B. | 用小苏打治疗胃酸过多:HCO3-+H+═CO2↑+H2O | |
| C. | 氯化铝溶液中加入过量氨水:Al3++3OH-═Al(OH)3↓ | |
| D. | 三氯化铁溶液中加入铁粉:Fe3++Fe═2 Fe2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com