
【题目】下列说法正确的是( )
A. 有机物的同系物具有相同的通式,且组成相差n(n>0的正整数)个CH2原子团,因此等质量的同系物完全燃烧时消耗氧气的物质的量相差1.5nmol
B. 根据卤代烃的消去反应一定能判断卤代烃中所含卤素原子的种类
C. 饱和一元醇可在一定条件下与氢卤酸发生取代反应
D. 分子式为C7H16的有机物中有三种不同化学环境的氢原子,此有机物一定是2,4―二甲基戊烷或3,3―二甲基戊烷
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某氯化镁溶液的密度为1.18 g·cm-3,其中镁离子的质量分数为5.1%。300 mL该溶液中氯离子的物质的量约等于( )
A. 0.37 mol B. 0.63 mol C. 0.74 mol D. 1.5 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容中发生下列反应aA(g)![]() cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是( )
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是( )
A. A的转化率变大 B. 平衡向正反应方向移动
C. D的体积分数变大 D. a < c+d
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、为了研究化学反应A+B=C+D的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。试回答下列问题:
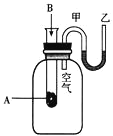
(1)该反应为________反应(填“放热”或“吸热”)。
(2)A和B的总能量比C和D的总能量_________(填“高”或“低”)。
(3)该反应的物质中的化学能通过化学反应转化成________释放出来。
(4)该反应的反应物化学键断裂吸收的能量________(填“高”或“低”)于生成物化学键形成放出的能量。
(5)Ⅱ、同素异形体相互转化的反应热相当小,而且转化速率较慢,有时还很不完全,测定反应热很困难。现在可根据盖斯提出的“不管化学过程是一步完成还是分几步完成,这个总过程的热效应是相同的”观点来计算反应热。
已知:
①P4(白磷,s)+5O2(g)= P4O10(s) ΔH=-2983.2 kJ·mol1
②P(红磷,s)+5/4O2(g)=1/4P4O10(s) ΔH=-738.5 kJ·mol1
则白磷转化为红磷的热化学方程式为__________。相同状况下,能量状态较低的是________;白磷的稳定性比红磷_________(填“高”或“低”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁为中学常见物质,其中甲、乙为单质,丙为氧化物,它们之间存在如图所示的转化关系:

下列说法正确的是( )
A. 若甲、乙元素是同主族元素,根据元素周期表推测,此时乙单质可能是Si
B. 若甲、乙均为金属单质,则丁所属的物质类别一定是碱性氧化物
C. 若甲为金属单质,乙为非金属单质,则甲只能是Mg
D. 若甲、乙元素是同周期元素,则该反应的化学方程式一定为:2F2 + 2H2O=4HF + O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是
A. 电解饱和食盐水可制取烧碱、氯气、氢气
B. 从海水中可提取镁、溴、碘等物质
C. 粗铜(含少量Zn、Fe、Pt等)电解精炼后,溶液中金属阳离子只有Fe2+、Zn2+
D. 在镀件上镀铜,镀件作阴极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国科学技术名词审定委员会已确定第116号元素Lv的名称为鉝。关于![]() 的叙述错误的是( )
的叙述错误的是( )
A. 原子序数116B. 中子数177
C. 核外电子数116D. 相对原子质量293
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究物质的合成或制备是有机化学、无机化学的重要任务之一。
(1)某实验小组探究实验室制备无水氯化镁的方法,设计了如下图装置。
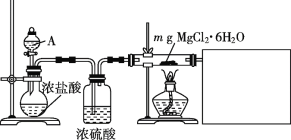
①分液漏斗中的A物质是___________ (填试剂名称)。
②利用中学常见的仪器,某同学在空白方框内补充完整实验装置,他选择的试剂有____ (填序号)
A.稀NaOH溶液 B.无水氯化钙 C.稀硫酸 D.浓硫酸
(2)实验室制备并收集纯净乙烯。
①有的同学通过乙醇制备乙烯,写出相关化学方程式:_______________;该实验除乙醇外,所需的试剂或用品(不包括仪器)有_______________________。
②有的同学探究其他制备乙烯的方法,他设计了下图装置制备乙烯。实验结果是量筒内壁附着较多无色油状液体,且得到很少量的气体。请分析气体产率很低的原因主要是_______。
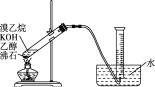
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁与4mol·L-1的稀硫酸反应(放热反应)生成H2的物质的量与反应时间的关系如图所示。下列结论正确的是

A.反应开始2min内平均反应速率最大
B.常温下,改用98.3%的浓硫酸可以加快反应速率
C.反应在2~4min间生成H2的平均反应速率为0.1mol·L-1·min-1
D.2~4min内反应速率逐渐增大,说明2~4min内温度比浓度对反应速率的影响大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com